Нарушаване на концентрационната функция на бъбреците. Функционални тестове за оценка на концентрационната функция на бъбреците
Прочетете също
Структурната единица на бъбреците е нефронът, който отговаря за процеса на филтриране на кръвта. В двата пикочни органа са събрани около два милиона нефрона, които са сплетени на групи в малки топчета. Това е гломерулният апарат (гломерулен), в който се извършва гломерулната филтрация на бъбреците.
Важно: през деня през гломерулите на нефрона преминават от 120 до 200 литра кръв. В същото време именно в нефроните се извършва разделянето на всички токсини и разпадни продукти на протеини, въглехидрати и мазнини.
Принципът на процеса на филтриране
Процесът на филтриране на бъбреците е доста прост и ясен. Първо, кръвта, обогатена с кислород и други хранителни вещества, навлиза в бъбреците, а именно в гломерулния апарат. В нефроните, които имат вид "сито", има отделяне на токсични вещества и други продукти на разпадане от водата. След такова разделяне водата и полезните микроелементи (глюкоза, натрий, калий) се абсорбират обратно. Тоест протича процесът на реабсорбция. И всички токсини продължават движението си през тубулите на нефрона към бъбречните пирамиди и по-нататък в пиелокалцеалната система. Тук вече се образува вторична урина, която излиза през уретерите, пикочния мехур и уретрата.
Важно: струва си да знаете, че ако бъбреците на човек са болни, тогава нефроните в тях бавно умират един по един. Така филтриращата функция на пикочните органи постепенно намалява. Трябва да се помни, че нефроните, подобно на нервните клетки, не могат да бъдат възстановени. И тези нефрони, които поемат двойно и тройно натоварване, в крайна сметка престават да се справят с функцията си и скоро се провалят.
Фактори, които могат да повлияят на промяната на GFR

Скоростта на филтрация в гломерулния апарат зависи от такива фактори:
- Скоростта на транспортиране на плазмата през бъбречния гломерулен апарат. Тоест това означава обемът кръв, преминаващ през лумбалната артериола за определена единица време. Обикновено тази цифра е 600 ml / min за човек със средно тегло 70 kg.
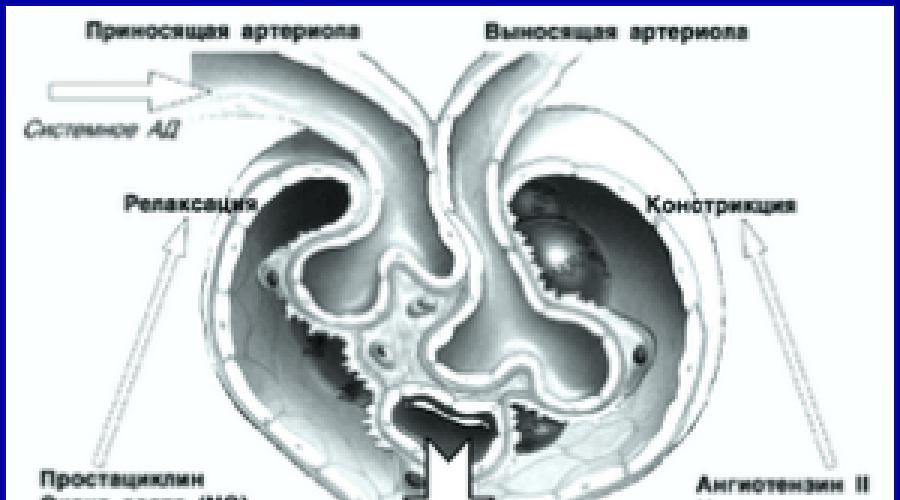
- Индикатор за налягането в съдовата система на тялото. Нормалното и здраво тяло се характеризира с по-високо налягане в отвеждащия съд, отколкото в изходящия съд. В противен случай процесът на филтриране ще бъде труден и скоростта му ще бъде намалена.
- Броят на здравите нефрони. Колкото повече бъбрекът е засегнат от патологичното състояние, толкова по-малка става филтриращата площ. Тоест броят на здравите нефрони намалява.
Оценка на GFR
blockquoteblue>Важно: обикновено бъбречната филтрация в здрави органи се извършва с постоянна скорост и остава непроменена до развитието на патологични процеси в пикочните органи.
Патологии, които определят GFR

Патологичните процеси, които променят скоростта на гломерулната филтрация на бъбреците до по-ниска страна, могат да бъдат много разнообразни. По-специално, GFR се влияе от такива патологии и заболявания:
- Хронична бъбречна недостатъчност. В този случай в урината ще се забележи и повишена концентрация на креатинин и урея. Тоест бъбреците не се справят с филтриращата си функция.
- пиелонефрит. Това възпалително и инфекциозно заболяване засяга предимно тубулите на нефрона. И едва тогава настъпва спадът на GFR.
- Диабет. А също и при хипертония (високо кръвно налягане), лупус еритематозус се наблюдава повишена скорост на процеса на бъбречна филтрация.
- Хипотония (ниско кръвно налягане). Както и състояние на шок и сърдечна недостатъчност може да провокира намаляване на GFR до значителни граници.
Помощ при диагностициране на заболявания

Измерването на GFR позволява да се идентифицират различни заболявания и патологични състояния на ранен етап. В същото време, за да се проследи процесът на филтриране в бъбреците, често се използва методът за въвеждане на инулин в кръвта, специално контролно вещество, което се екскретира през гломерулния апарат. Инулинът се прилага непрекъснато по време на изследването, за да се поддържа постоянна концентрация в кръвта.
Вземането на проби от урина за анализ при поддържане на нивото на инулин се извършва четири пъти с интервал от половин час. Но си струва да знаете, че този метод за анализ на състоянието на бъбреците е доста сложен и е приложим изключително за научни цели.
Също така е възможно да се оцени GFR чрез нивото на креатининовия клирънс, което пряко зависи от чистата телесна маса на пациента. Тук си струва да знаете, че при активните мъже креатининовият клирънс е значително по-висок, отколкото при жените и децата. Обърнете внимание, че креатининът излиза от тялото изключително през гломерулния апарат. Следователно, ако процесът на филтриране в бъбреците е нарушен, концентрацията на креатинин в урината се повишава и е 70% в сравнение с GFR.
Важно: когато провеждате тест за урина за креатинин, трябва да знаете това лекарстваможе значително да изкриви резултата. Нормално нивото на креатинина при мъжете е 18-21 mg/kg, а при жените 15-18 mg/kg. Ако индикаторите са намалени, това може да означава неизправност в бъбреците.

Тази техника за изследване на работата на пикочните органи се извършва по следния начин:
- Сутринта на пациента се предлага да изпие половин литър вода на празен стомах. След това той трябва да уринира на всеки час, за да събере части от биоматериала в отделни контейнери.
- При уриниране пациентът е длъжен да отбелязва часа на началото и края на акта.
- И в интервала между вземането на порции урина, кръвта се взема от пациента от вената, за да се определи креатининовият клирънс. Изчислява се по специална формула. Формулата за изчисление изглежда така - F1=(u1/p)v1.
Тук значенията са както следва:
- Fi е гломерулна филтрация (нейната скорост);
- U1 - съдържанието на контролното вещество в кръвта;
- Vi - времето на първото уриниране след пиене на вода (в минути)
- p е концентрацията на креатинин в кръвната плазма.
Изчислете креатининовия клирънс, като използвате горната формула на всеки час. В този случай изчисленията се извършват през деня.
Това е интересно: при нормалните мъже GFR е 125 литра / мин, а при жените - 110 мл / мин.
Изчисляване на GFR при деца

За да изчислите скоростта на гломерулна филтрация при деца, използвайте формулата на Шварц. В първия случай се взема кръвна проба от вената на малък пациент на празен стомах. Необходимо е да се определи нивото на креатинин в кръвната плазма. На фона на биоматериала, взет от бебето, се събират и две порции урина на всеки час. И също така отбележете продължителността на акта на уриниране в минути или секунди. Изчисленията, използващи формулата на Шварц, позволяват да се получат две стойности на GFR.
За втория метод на изчисление дневният обем на урината се събира от малък пациент на интервали от час. Тук обемът трябва да бъде най-малко 1,5 литра. Ако по време на изчисленията резултатът от скоростта на гломерулна филтрация е 15 ml / min (т.е. тя е силно намалена), тогава това показва бъбречна недостатъчност или хронично бъбречно заболяване.
Важно: GFR не винаги може да падне на фона на смъртта на нефрона. Често скоростта на филтриране може да намалее на фона на възпалителен процес, протичащ в бъбреците. Ето защо при първите подозрителни симптоми (болка в долната част на гърба, тъмна урина, подуване) е необходимо спешно да се свържете с нефролог или уролог.
Лечение на бъбреците и възстановяване на скоростта на филтрация
В случай на нарушение на филтрационната функция на бъбреците, лечението трябва да се предписва само от специалист, в зависимост от основната причина, довела до патологията. В повечето случаи лекарствата "Theobromine" и "Eufillin" помагат за подобряване на ситуацията. Те повишават диурезата, което води до нормализиране на GFR.
Също така, на фона на лечението е необходимо да се спазва диета и режим на пиене. Струва си да пиете до 1,2 литра течност на ден. И от диетата трябва да се изключат всички пържени, мазни, солени, пикантни, пушени. Ще бъде по-добре, ако пациентът премине на пара и варени ястия по време на лечението.
Ако лекуващият лекар разреши, тогава можете да регулирате скоростта на гломерулната филтрация и народни средства. По този начин обикновеният магданоз, който подобрява диурезата, е известно от дълго време, че повишава GFR. Сухите му семена и корени (в количество 1 супена лъжица) се запарват с вряла вода (500 мл) и се оставят да се държат 2-3 часа. След това настойката се прецежда и се пие на два пъти през деня по 0,5 чаши.
За повишаване на GFR може да се използва и корен от шипка. Тя е в размер на 2 с.л. залейте с вряща вода и гответе на слаб огън за 15 минути. След това бульонът се филтрира и се пие по 70 ml три пъти на ден. Такова лекарство също увеличава диурезата, което определено ще увеличи GFR.
Важно е да знаете, че само специалист трябва да контролира целия процес на лечение. Самолечението е строго забранено.
lecheniepochki.ru
Филтриране на кръвта в бъбреците
За да разберете механизма на пречистване на кръвта и образуване на урина, трябва да имате представа за структурата на бъбреците. Този сдвоен орган се състои от огромен брой нефрони, в които се образува урина.
Основните бъбречни функции са:
уриниране; Пречистване на кръвта, отделяне на лекарства, метаболити и др.; Регулиране на електролитния метаболизъм; Контрол на налягането и обема на циркулиращата кръв; Поддържане на киселинно-базовия баланс.
Всъщност бъбреците са непрекъснато работещи филтри, които обработват до 1,2 литра кръв в минута.
Всеки бъбрек има форма на боб. На всеки бъбрек има вид вдлъбнатина, която също се нарича порта. Те водят до запълнено с мазнини пространство или синус. Там също се намират пиелокалицеалната система, нервните влакна и съдовата система. От същата порта излизат вената и артерията на бъбрека, както и уретера.
Всеки бъбрек се състои от множество нефрони, които представляват комплекс от тубули и гломерули. Филтрирането на кръвта се извършва директно в бъбречното телце или гломерула. Това е мястото, където урината се филтрира от кръвта и отива в пикочния мехур.
Във видеото структурата на бъбреците
Къде се случва
Бъбрекът, така да се каже, е поставен в капсула, под която има гранулиран слой, наречен кортекс, а под него е медулата. Медулата се развива в бъбречни пирамиди, между които има колони, разширяващи се към бъбречните синуси. На върховете на тези пирамиди има папили, които изпразват пирамидите, пренасяйки съдържанието им в малки чаши, след това в големи.
Броят на чашките може да е различен за всеки човек, въпреки че обикновено 2-3 големи чашки се разклоняват на 4-5 малки чашки, като една малка чашка задължително обгражда папилата на пирамидата. От малката чашка урината навлиза в голямата чашка и след това в структурите на уретера и пикочния мехур.
Кръвта на бъбреците се доставя от бъбречната артерия, която се разклонява на по-малки съдове, след което кръвта навлиза в артериолите, които се разделят на 5-8 капиляра. Така че кръвта навлиза в гломерулната система, където се извършва процесът на филтриране.
Схема на бъбречна филтрация 
Гломерулна филтрация - Определение
Филтрирането в гломерулите на бъбреците се извършва по прост принцип:
Първо, течността се изстисква/филтрира от гломерулните мембрани под хидростатично налягане (≈125 ml/min); След това филтрираната течност преминава през нефроните, по-голямата част от нея под формата на вода и необходими елементи се връща в кръвта, а останалата част се образува в урината; Средната скорост на образуване на урина е около 1 ml / min.
Бъбречният гломерул филтрира кръвта, изчиствайки я от различни протеини. В процеса на филтриране се образува първична урина.
Основната характеристика на процеса на филтриране е неговата скорост, която се определя от фактори, които влияят на бъбречната дейност и общото здравословно състояние на човека.
Скоростта на гломерулна филтрация е обемът на първичната урина, образувана в бъбречните структури за минута. Нормалната скорост на филтриране е 110 ml/min за жени и 125 ml/min за мъже. Тези показатели действат като своеобразен еталон, който подлежи на корекция в съответствие с теглото, възрастта и други показатели на пациента.
Схема на гломерулна филтрация 
Нарушения на филтрацията
През деня нефроните филтрират до 180 литра първична урина. Цялата кръв в тялото има време да се пречисти от бъбреците 60 пъти на ден.
Но някои фактори могат да провокират нарушение на процеса на филтриране:
намаляване на налягането; нарушения на пикочните пътища; Стесняване на артерията на бъбрека; Травматизация или увреждане на мембраната, която изпълнява филтриращи функции; Повишено онкотично налягане; Намаляване на броя на "работещите" гломерули.
Такива условия най-често причиняват нарушения на филтрацията.
Как да идентифицираме нарушение
Нарушаването на филтрационната активност се определя чрез изчисляване на нейната скорост. Възможно е да се определи колко филтрация е ограничена в бъбреците, като се използват различни формули. Като цяло процесът на определяне на скоростта се свежда до сравняване на нивото на определено контролно вещество в урината и кръвта на пациента.
Обикновено инулинът, който е фруктозен полизахарид, се използва като сравнителен стандарт. Концентрацията му в урината се сравнява със съдържанието в кръвта и след това се изчислява съдържанието на инсулин.
Колкото повече инулин е в урината спрямо нивото му в кръвта, толкова по-голям е обемът на филтрираната кръв. Този показател се нарича още инулинов клирънс и се счита за стойността на пречистената кръв. Но как да изчислим скоростта на филтриране?
Формулата за изчисляване на скоростта на гломерулна филтрация на бъбреците е следната:
GFR (ml/min),
където Min е количеството инулин в урината, Pin е съдържанието на инулин в плазмата, Vurine е обемът на крайната урина и GFR е скоростта на гломерулна филтрация.
Бъбречната активност може също да се изчисли с помощта на формулата на Cockcroft-Gault, която изглежда така:
При измерване на филтрацията при жени резултатът трябва да се умножи по 0,85.
Доста често в клиничните условия креатининовият клирънс се използва за измерване на GFR. Подобно изследване се нарича още тест на Rehberg. Рано сутрин пациентът изпива 0,5 литра вода и веднага изпразва пикочния мехур. След това на всеки час трябва да уринирате, като събирате урина в различни контейнери и отбелязвате продължителността на всяко уриниране.
След това се изследва венозна кръв и се изчислява гломерулната филтрация по специална формула:
Fi \u003d (U1 / p) x V1,
където Fi е гломерулна филтрация, U1 е съдържанието на контролния компонент, p е нивото на креатинина в кръвта, а V1 е продължителността на изследваното уриниране. По тази формула всеки час се прави изчисление през целия ден.
Симптоми
Признаците на нарушена гломерулна филтрация обикновено се свеждат до промени в количествения (увеличаване или намаляване на филтрацията) и качествения (протеинурия) характер.
Допълнителните функции включват:
Спад на налягането; бъбречна стаза; Хипередем, особено в крайниците и лицето; Нарушения на уринирането като намалено или повишено желание, поява на нехарактерна утайка или промени в цвета; Болка в лумбалната област Натрупване в кръвта на различни видове метаболити и др.
Спад на налягането обикновено се случва при шокови състояния или миокардна недостатъчност.
Симптоми на нарушена гломерулна филтрация в бъбреците 
Как да подобрим филтрирането
Възстановяването на филтрацията на бъбреците е от съществено значение, особено ако има персистираща хипертония. Заедно с урината излишните електролити и течности се измиват от тялото. Именно тяхното забавяне причинява повишаване на кръвното налягане.
За подобряване на бъбречната функция, по-специално гломерулната филтрация, специалистите могат да предписват лекарства като:
Теоброминът е слаб диуретик, който чрез увеличаване на бъбречния кръвен поток повишава филтрационната активност; Eufillina също е диуретик, съдържащ теофилин (алкалоид) и етилендиамид.
В допълнение към приемането на лекарства е необходимо да се нормализира общото благосъстояние на пациента, да се възстанови имунитетът, да се нормализира кръвното налягане и др.
За да се възстанови функцията на бъбреците, също е необходимо да се храните балансирано и да спазвате дневния режим. Само интегриран подход ще помогне за нормализиране на филтрационната активност на бъбреците.
Не е лоша помощ за увеличаване на бъбречната дейност и народни методикато диета с диня, отвара от шипка, диуретични отвари и билкови отвари, чайове и др. Но преди да предприемете нещо, трябва да се консултирате с нефролог.
Гломерулната филтрация е една от основните характеристики, които отразяват дейността на бъбреците. Филтриращата функция на бъбреците помага на лекарите при диагностицирането на заболявания. Скоростта на гломерулна филтрация показва дали има увреждане на гломерулите на бъбреците и степента на тяхното увреждане, определя тяхната функционалност. В медицинската практика има много методи за определяне на този показател. Нека да видим каква е тяхната същност и кои от тях са най-ефективни.

Какво е?
В здраво състояние структурата на бъбреците има 1-1,2 милиона нефрони (компоненти на бъбречната тъкан), които комуникират с кръвния поток чрез кръвоносните съдове. В нефрона има гломерулно натрупване на капиляри и тубули, които участват пряко в образуването на урина - те пречистват кръвта от метаболитни продукти и коригират нейния състав, тоест филтрират първичната урина. Този процес се нарича гломерулна филтрация (CF). На ден се филтрират 100-120 литра кръв.
 Диаграма на гломерулната филтрация на бъбреците.
Диаграма на гломерулната филтрация на бъбреците.
Скоростта на гломерулна филтрация (GFR) често се използва за оценка на бъбречната функция. Той характеризира количеството първична урина, произведена за единица време. Нормата на показателите за скорост на филтриране е в диапазона от 80 до 125 ml / min (жени - до 110 ml / min, мъже - до 125 ml / min). При по-възрастните хора процентът е по-нисък. Ако възрастен има GFR под 60 ml / min, това е първият сигнал на тялото за началото на развитието на хронична бъбречна недостатъчност.
Назад към индекса
Фактори, които променят скоростта на гломерулна филтрация на бъбреците
Скоростта на гломерулна филтрация се определя от няколко фактора:
Скоростта на плазмения поток в бъбреците е количеството кръв, което протича за единица време през аферентната артериола в бъбречния гломерул. Нормалният показател, ако човек е здрав, е 600 ml / min (изчислението е направено въз основа на данни за средно лице с тегло 70 kg) Ниво на налягане в съдовете. Обикновено, когато тялото е здраво, налягането в аферентния съд е по-високо, отколкото в еферентния. В противен случай процесът на филтриране не се случва Броят на здравите нефрони. Има патологии, които засягат клетъчната структура на бъбрека, в резултат на което се намалява броят на способните нефрони. Подобно нарушение допълнително води до намаляване на площта на филтриращата повърхност, от размера на която директно зависи GFR.
Тест на Реберг-Тареев
 Надеждността на пробата зависи от времето, когато е събран анализът.
Надеждността на пробата зависи от времето, когато е събран анализът.
Тестът на Reberg-Tareev изследва нивото на клирънс на креатинин, произведен от тялото - обемът на кръвта, от който е възможно да се филтрира 1 mg креатинин за 1 минута от бъбреците. Креатининът може да се измери в съсирена плазма и урина. Надеждността на изследването зависи от времето, когато е събран анализът. Проучването често се провежда по следния начин: урината се събира в продължение на 2 часа. Той измерва нивото на креатинина и минутната диуреза (обемът на урината, който се образува за минута). GFR се изчислява въз основа на получените стойности на тези два показателя. По-рядко използван метод е събирането на урина на ден и 6-часови проби. Независимо коя техника използва лекарят, пациентът е сутрин, докато не закуси, вземете кръв от вената, за да проведете изследване на креатининовия клирънс.
Тест за креатининов клирънс се предписва в такива случаи:
болка в областта на бъбреците, подуване на клепачите и глезените; нарушено отделяне на урина, тъмна урина с кръв; необходимо е да се установи правилната доза лекарства за лечение на бъбречни заболявания; диабет тип 1 и тип 2; хипертония; абдоминално затлъстяване, синдром на инсулинова резистентност; злоупотреба с тютюнопушене; сърдечно-съдови заболявания; преди операция; хронично бъбречно заболяване. Назад към съдържанието
Тест на Кокрофт-Голд

Тестът Cockcroft-Gold също установява концентрацията на креатинин в кръвния серум, но се различава от описания по-горе метод за събиране на материали за анализ. Тестът се провежда по следния начин: сутрин на празен стомах пациентът изпива 1,5-2 чаши течност (вода, чай), за да активира производството на урина. След 15 минути пациентът облекчава малка нужда в тоалетната, за да изчисти пикочния мехур от остатъците от образувания по време на сън. Следва мир. Един час по-късно се взема първата проба от урина и се записва нейното време. Втората порция се събира в следващия час. Между това пациентът взема кръв от вената в 6-8 ml. Освен това, според получените резултати, се определя креатининовият клирънс и количеството урина, което се образува за минута.
Назад към индекса
Скорост на гломерулна филтрация според формулата MDRD
Тази формула отчита пола и възрастта на пациента, така че с негова помощ е много лесно да се наблюдава как бъбреците се променят с възрастта. Често се използва за диагностициране на бъбречна дисфункция при бременни жени. Самата формула изглежда така: GFR \u003d 11,33 * Crk - 1,154 * възраст - 0,203 * K, където Crk е количеството креатинин в кръвта (mmol / l), K е коефициент, зависим от пола (за жени - 0,742 ). В случай, че този показател в заключението на анализа е даден в микромола (µmol / l), тогава неговата стойност трябва да бъде разделена на 1000. Основният недостатък на този метод на изчисление е неправилните резултати при повишен CF.
Назад към индекса
Причини за намаляване и увеличаване на показателя

Има физиологични причини за промени в GFR. По време на бременност нивото се покачва, а с напредването на възрастта на организма намалява. Храните с високо съдържание на протеини също могат да провокират увеличаване на скоростта. Ако човек има патология на бъбречната функция, тогава CF може както да се увеличи, така и да намали, всичко зависи от конкретното заболяване. GFR е най-ранният предиктор за увредена бъбречна функция. Интензитетът на CF намалява много по-бързо, отколкото се губи способността на бъбреците да концентрират урината и азотните отпадъци се натрупват в кръвта.
Когато бъбреците са болни, намалената филтрация на кръвта в бъбреците се провокира от нарушения в структурата на органа: броят на активните структурни единици на бъбреците намалява, коефициентът на ултрафилтрация намалява, настъпват промени в бъбречния кръвен поток, филтриращата повърхност намалява , настъпва обструкция на бъбречните тубули. Причинява се от хронични дифузни, системни бъбречни заболявания, нефросклероза на фона на артериална хипертония, остра чернодробна недостатъчност, тежко сърдечно заболяване, чернодробно заболяване. В допълнение към бъбречните заболявания, GFR се влияе от екстраренални фактори. Намаляване на скоростта се наблюдава заедно със сърдечна и съдова недостатъчност, след пристъп на тежка диария и повръщане, с хипотиреоидизъм, рак на простатата.
Повишената GFR е по-рядко срещана, но се появява, когато диабетв ранните стадии, хипертония, системно развитие на лупус еритематозус, в началото на развитието на нефротичен синдром. Също така, лекарства, които влияят на нивото на креатинина (цефалоспорин и подобни по ефект върху тялото), могат да увеличат честотата на CF. Лекарството повишава концентрацията си в кръвта, така че при вземане на анализа се откриват фалшиво повишени резултати.
Назад към индекса
стрес тестове
 Зареждането с протеини е консумацията на необходимото количество месо.
Зареждането с протеини е консумацията на необходимото количество месо.
В основата на стрес тестовете е способността на бъбреците да ускоряват гломерулната филтрация под въздействието на определени вещества. С помощта на такова изследване се определя CF резервът или бъбречният функционален резерв (RFR). За разпознаването му се прилага еднократно (остро) натоварване с протеин или аминокиселини или те се заместват с малко количество допамин.
Зареждането с протеини е промяна в диетата. Необходимо е да се консумират 70-90 грама протеин от месо (1,5 грама протеин на 1 килограм телесно тегло), 100 грама растителни протеини или да се въведе интравенозно набор от аминокиселини. При хора без здравословни проблеми има 20-65% увеличение на GFR още 1-2,5 часа след приема на доза протеини. Средната стойност на PFR е 20-35 ml на минута. Ако увеличението не се случи, тогава най-вероятно пропускливостта на бъбречния филтър е нарушена при човек или се развиват съдови патологии.
Назад към индекса
Значението на изследванията
Важно е да се наблюдава GFR за хора със следните състояния:
хроничен и остър ход на гломерулонефрит, както и неговата вторична поява; бъбречна недостатъчност; възпалителни процеси, провокирани от бактерии; увреждане на бъбреците в резултат на системен лупус еритематозус; нефротичен синдром; гломерулосклероза; бъбречна амилоидоза; нефропатия при диабет и др.
Тези заболявания причиняват намаляване на GFR много преди проявата на функционални нарушения на бъбреците, повишаване на нивото на креатинин и урея в кръвта на пациента. В пренебрегвано състояние болестта провокира необходимостта от бъбречна трансплантация. Следователно, за да се предотврати развитието на всякакви патологии на бъбреците, е необходимо редовно да се провеждат изследвания на тяхното състояние.
no-gepatit.ru
Ултрафилтрацията на плазмата с образуването на първична урина се извършва в гломерулите на бъбреците.
Филтриращата мембрана на гломерула се състои от три слоя: капилярен ендотел, базална мембрана и епителни клетки от вътрешната част на капсулата, които се наричат подоцити. Подоцитите имат процеси, които плътно прилягат към базалната мембрана. Структурата на базалната мембрана е сложна, по-специално съдържа мукополизахариди и колагенов протеин. Пропускливостта на гломерулния филтър зависи основно от състоянието на базалната мембрана, тъй като нейните отвори са най-малки, от порядъка на 5 нанометра (според Rouyet).
Филтриращата мембрана на гломерула е способна да пропуска почти всички вещества, присъстващи в плазмата с молекулно тегло под 70 000, както и малка част от албумините. При определени условия през бъбречния филтър преминават и по-големи белтъчни молекули, например антигени на коремен тиф и дизентерия, вирус на грип, морбили и др.
Гломерулната филтрация се определя от филтрационното налягане (PD). Нормално PD = 75-(25+10) = 40 mmHg чл., където 75 mm Hg. Изкуство. - хидростатично налягане в капилярите на гломерулите; 25 mmHg Изкуство. - онкотично налягане на плазмените протеини; 10 mmHg Изкуство. - вътребъбречно налягане. Налягането на филтриране може да варира в рамките на 25-50 mm Hg. Изкуство. Приблизително 20% от кръвната плазма, преминаваща през гломерулните капиляри, се подлага на филтрация (филтрационна фракция).
§ 304 Индекс на пречистване (клирънс)
За определяне на филтрационния капацитет на бъбреците се използва дефиницията на индекса на пречистване. Индикаторът за пречистване или клирънс (от английското clear - изчистване) е обемът на кръвната плазма, който се освобождава напълно от бъбреците от това вещество за 1 минута. Клирънсът се определя от отстраняването на ендогенни вещества, циркулиращи в кръвта (например ендогенен креатинин) или чрез отстраняване на вещества, специално въведени в кръвта (например инулин и др.). За да изчислите клирънса, трябва да знаете съдържанието на веществото в кръвта (K), съдържанието му в урината (M) и минутната диуреза (D) - количеството урина, освободено за 1 минута. Клирънсът (C) се изчислява по формулата:
Скоростта на пречистване не е еднаква за различните вещества. Например, средният клирънс на инулин (полизахарид) е 120 ml / min, урея - 70 ml / min, фенол рота - 400 ml / min и др. Тази разлика се обяснява с факта, че инулинът се екскретира чрез филтриране и не реабсорбиран обратно; уреята се филтрира, но частично се реабсорбира, а фенолът се екскретира чрез активна секреция в тубулите и частично се филтрира.
За да се определи истинският капацитет на филтриране на гломерулите, т.е. количеството първична урина, образувана за 1 минута, е необходимо да се използват вещества, които се освобождават само чрез филтриране и не се реабсорбират в тубулите. Те включват вещества без праг, като инулин и хипосулфит. При възрастен човек стойността на гломерулната филтрация (първичен обем на урината) е средно 120 ml / min, т.е. 150-170 l / ден. Намаляването на този показател показва нарушение на филтрационната функция на бъбреците.
§ 305. Ефективност на бъбречния кръвоток
Индексът на клирънс на пара-аминохипуровата киселина (PAH) дава възможност да се определи ефективността на бъбречния кръвен поток. Това вещество навлиза в урината чрез активна секреция и кръвта, изтичаща от бъбрека, не съдържа PAH. Следователно скоростта на пречистване на ПАХ съответства на обема на кръвната плазма, преминала през съдовете на бъбреците за 1 минута. Тя е равна на средно 650 ml / min. Обемът на кръвта, а не плазмата, която е преминала през бъбреците, може да се определи чрез коригиране на хематокрита (обикновено обемът на червените кръвни клетки е 45%, плазмата - 55%). След като се направи пропорция, се изчислява бъбречният кръвен поток: 660 ml - 55%, X-100%, X = 1200 ml / min.
Трябва да се има предвид, че клирънсът на ПАХ не винаги е адекватен на бъбречния кръвоток. Коефициентът на клирънс на PAH може да намалее при непроменен бъбречен кръвоток, ако процесите на секреция са нарушени поради значително увреждане на тубулите (хроничен нефрит, нефроза и др.).
Устойчиво намаляване на ефективността на бъбречния кръвен поток се наблюдава при хипертония и също ранен знакразвитие на бъбречна артериосклероза.
§ 306. Нарушение на гломерулната филтрация
Намалена филтрация.Намаляването на първичното производство на урина зависи от редица екстраренални и бъбречни фактори. Те включват:
- спад на кръвното налягане [покажи]
- стесняване на бъбречната артерия и артериолите [покажи]
- повишено онкотично кръвно налягане [покажи]
- запушване на изтичането на урина [покажи]
- намаляване на броя на функциониращите гломерули [покажи]
- повреда на филтърната мембрана [покажи]
Прогресивното намаляване на броя на функциониращите нефрони е типично за хронично бъбречно заболяване с дифузно бъбречно увреждане. Те включват хроничен гломерулонефрит, артериосклероза на бъбреците, пиелонефрит и др. Тези заболявания са придружени от склероза на гломерулите и смърт на нефроните, завършващи с набръчкване на бъбреците. С намаляване на броя на активните нефрони до 1/10-1/20 от нормалния им размер, филтрацията спира, развива се тежка уремия (виж § 314).
Увеличаване на гломерулната филтрациявидяно с:
- повишен тонус на еферентната артериола. Спазъм на еферентната артериола и повишаване на филтрацията се отбелязват при въвеждането на малки дози адреналин (надбъбречна полиурия) в началния стадий на хипертония.
- намален тонус на аферентната артериола. Тонът на адукторната артериола може да намалее рефлексивно поради ограничаване на кръвообращението в периферията на тялото, например по време на треска (повишена диуреза по време на етапа на повишаване на температурата).
- намаляване на онкотичното кръвно налягане. Повишена филтрация поради спад на онкотичното налягане се отбелязва при обилно приложение на течности или поради разреждане на кръвта (по време на спадане на отока).
§ 307. Нарушаване на тубулната реабсорбция
Епителните клетки на различните части на тубулите имат високоспециализирани функции. Те съдържат различни ензими и молекули-носители, участващи в транспорта на вещества от тубулите в кръвта (реабсорбция) и от кръвта в лумена на тубулите (секреция). Тези процеси протичат активно срещу висок концентрационен градиент и с голям разход на енергия за клетъчно дишане.
Най-честите механизми на нарушена тубулна реабсорбция включват:
- пренапрежение на процесите на реабсорбция и изчерпване на ензимните системи поради излишък на реабсорбирани вещества в първичната урина;
- намаляване на активността на ензимите на тубуларния апарат: а) наследствен дефект в ензимите, които осигуряват реабсорбцията на определени вещества или б) блокада на ензими от инхибитори;
- структурно увреждане на тубулите (дистрофия, некроза) при инфекциозни и възпалителни процеси, нарушения на кръвоснабдяването на бъбреците, особено на кортикалния кръвоток, и отравяне с отрови.
- Нарушена реабсорбция на глюкоза [покажи]
- Нарушена реабсорбция на протеини [покажи]
- Нарушена реабсорбция на аминокиселини [покажи]
- Нарушена реабсорбция на натрий [покажи]
- Нарушение на реабсорбцията на вода [покажи]
§ 308. Нарушаване на способността на бъбреците да концентрират и разреждат урината
Човешките бъбреци са в състояние да отделят урина 4 пъти по-хипертонична и 6 пъти по-хипотонична от плазмата. При нормални условия концентрацията на вещества в крайната урина е многократно по-висока от концентрацията им в плазмата (Таблица 31).
Концентрационната способност на бъбреците може да се съди по относителната плътност (специфично тегло) на урината. Но тези показатели не винаги съвпадат.
При здрав човек относителната плътност на урината с нормална диета не е по-ниска от 1,016-1,020 и варира в зависимост от приема на вода и водно-солевия баланс в рамките на 1,002-1,035 или повече. С възрастта осмотичната концентрация и относителната плътност на урината намаляват.
Неспособността на бъбреците да концентрират урината се нарича хипостенурия. Относителната плътност на урината спада до 1,012-1,006 и леко варира през деня (фиг. 77). Хипостенурията в комбинация с полиурия показва увреждане на тубулния апарат на бъбреците с относително достатъчна гломерулна функция (ранен стадий на хроничен нефрит, пиелонефрит). Хипостенурията в комбинация с олигурия показва участието на нарастващ брой гломерули в патологичния процес, в резултат на което се произвежда малко първична урина.
По-опасен признак на увреждане на бъбреците е изостенурията, когато относителната плътност на урината се доближава до относителната плътност на гломерулния филтрат (1,010) и не се променя (монотонна диуреза). Изостенурията показва нарушение на тубулната реабсорбция на вода и соли, загуба на способността на бъбреците да концентрират и разреждат урината. В резултат на разрушаването на епителните клетки, тубулите се превръщат в прости тръби, които пренасят гломерулния филтрат към бъбречното легенче. Комбинацията от изостенурия с олигурия е показател за тежка бъбречна недостатъчност.
§ 309. Нарушение на тубулната секреция
При заболявания на бъбреците процесите на секреция в тубулите могат да бъдат нарушени и всички вещества, секретирани чрез секреция, като антибиотици, йодсъдържащи контрастни вещества, се натрупват в кръвта.
Забавянето на пеницилин в кръвта и продуктите от неговите трансформации могат да имат токсичен ефект върху тялото. Ето защо при бъбречни заболявания пеницилинът, както и някои други антибиотици, трябва да се използва с повишено внимание.
Нарушението на секрецията на пикочна киселина възниква като наследствен дефект. Натрупването на пикочна киселина и соли на пикочната киселина в кръвта води до развитие на така наречената бъбречна подагра.
Повишена секреция на калий се наблюдава при излишък на хормона алдостерон и при употребата на диуретици - инхибитори на ензима карбоанхидраза. Загубата на калий (калиев диабет) води до хипокалиемия и тежка дисфункция.
Бъбреците изпълняват много ценна физиологична функция за поддържане на постоянно pH на кръвта. Тази функция е свързана най-вече с процесите на ацидогенеза и амониогенеза.
| Ацидогенеза - образуването на свободни Н + -йони в тубулните клетки и тяхната секреция в лумена на тубулите. Реакцията протича с участието на ензима карбоанхидраза (CO 2 + H 2 O карбоанхидраза -> H 2 CO 3 -> H + + HCO - 3. Амониогенезата е образуването на амоняк и амоний. Източникът на амоняк са аминокиселини, главно глутамин. След това се образува амониев йон: NH3 + H + -> NH4. Секрецията на Н + - йони създава условия за реабсорбция на натрия и бикарбоната и за отстраняване на киселинните продукти от тялото под формата на титруеми киселини. Водородните йони изместват натрия от съединения с аниони на слаби органични киселини и от фосфатен буфер. Амониевите йони изместват натрия от съединения със силни киселини. Натрият се абсорбира под формата на бикарбонат и се поддържа алкалният резерв на кръвта, а отделената урина е кисела (рН на урината обикновено е 5,5-6,5, но може да варира в зависимост от естеството на храната от 4,5 до 7,8). |
При нарушения на процеса на ацидо- и амониогенеза се губи голямо количество натрий и бикарбонати. Алкалните фосфати (Na 2 HPO 4) преобладават в урината вместо киселите (NaH 2 PO 4) и нейната реакция става алкална. При загуба на половината количество бикарбонати в кръвта се развива метаболитна ацидоза.
Причини за нарушена ацидогенеза и амониогенезаса:
- дългосрочно бъбречно заболяване с тежко увреждане или атрофия на тубулите;
- наследствен дефект в синтеза на ензимни системи, които осигуряват активна секреция на водородни йони (бъбречна тубулна ацидоза);
- приемане на някои диуретични лекарства - ензимни инхибитори на карбоанхидразата, като диакарб (предписани под наблюдението на лекар).
§ 310. Патологични съставки на урината при заболявания на бъбреците
до патологично съставни частиурината включва елементи, които не се срещат в урината на здрави хора, както и вещества, чието количество надвишава нормата. Въпреки това, не всяка промяна в състава на урината показва увреждане на бъбреците. Например, билирубин в урината се появява с чернодробна жълтеница, ацетон и захар - с диабет.
Най-честите симптоми на бъбречно заболяване са:
- Хематурия е появата на червени кръвни клетки в урината. Обикновено червените кръвни клетки не преминават през филтърната мембрана. При тежко увреждане (остър гломерулонефрит) еритроцитите проникват в капсулата на Боуман-Шумлянски и се екскретират в урината, която придобива червеникав оттенък. Червените кръвни клетки могат да навлязат в урината от уретерите (нараняване с движущи се камъни) или от Пикочен мехур(тумор, възпаление).
- Протеинурията е отделянето на протеин в урината. Бъбречната протеинурия възниква или поради увреждане на гломерулите, когато се увеличи тяхната пропускливост за протеини, или поради нарушение на реабсорбцията на протеини в тубулите (виж § 307).
- Левкоцитурия - наличие на левкоцити в урината (обикновено не повече от 1-3 от тях се откриват в седимента на урината в зрителното поле). Левкоцитурията е характерна за възпалителни процеси в бъбреците (пиелонефрит) и в пикочните пътища. Пиурия е изпускане на мътна урина с примес на гной и левкоцити.
- Цилиндрурия - появата на различни видове цилиндри в урината. Например, хиалиновите отливки са резултат от коагулация на протеини в лумена на тубулите по време на възпалителни и дистрофични процеси. Епителните и гранулираните отливки се състоят от дегенерирали тубулни епителни клетки.
- При нефролитиаза се появява утаяване на соли под формата на урати, оксалати и фосфати.
§ 311. Бъбречнокаменна болест
Бъбречнокаменната болест е следствие от нарушено отделяне на соли от бъбреците. Причината за това заболяване не е добре разбрана. Редица фактори допринасят за образуването на камъни в бъбреците: нарушение на минералния метаболизъм, инфекция на пикочните пътища, застой на урината, увреждане на бъбреците, липса на витамини А и D в храната, наследствен метаболитен дефект (оксалоза).
Камъните са съставени от фосфати (калциеви соли на фосфорната киселина), оксалати (калциеви соли на оксаловата киселина), урати (соли на пикочната киселина) и могат да имат смесен състав. Има цистинови камъни с наследствено заболяване (цистинурия), сулфаниламидни камъни с повишена концентрация на сулфаниламидни лекарства в урината, ксантинови камъни.
Според теорията на кристализацията камъните се образуват поради пренасищане на урината с кристалоиди и тяхното утаяване.
Според теорията на матрицата, солите са наслоени около скеле, състоящо се от протеини и въглехидрати (неразтворим мукополизахариден комплекс). Образуването му включва плазмени протеини, които интензивно проникват в капсулата с повишена пропускливост на гломерула, както и уромукоид, секретиран от епитела на тубулите поради тяхното дразнене. Органичната матрица се образува основно в тубулите в поне 95% от камъните. Растежът на камъка става чрез отлагане на редуващи се концентрични слоеве от мукополизахариди и кристалоиди върху него.
Камъните в бъбреците и утайките в урината имат различни форми и размери. Те се намират под формата на малки песъчинки или големи образувания, които изпълват кухината на таза.
Продължение: Глава 3. Бъбречна недостатъчност
bono-esse.ru
Структурата на нефрона
Урината е концентрат от вещества, чието отстраняване от тялото е необходимо за поддържане на постоянството на вътрешната среда. Това е един вид "загуба" на живот, включително токсични, чиято по-нататъшна трансформация е невъзможна, а натрупването е вредно. Функцията за отстраняване на тези вещества се изпълнява от пикочната система, основната част от която са бъбреците - биологични филтри. Кръвта преминава през тях, освобождавайки се от излишната течност и токсини.
На фиг. 1 схематично показва структурата на нефрона. А - бъбречно телце: 1 - аферентна артерия; 2- еферентна артерия; 3 - епителни листове на капсулата (външни и вътрешни); 4 - началото на тубула на нефрона; 5 - съдов гломерул. B - самият нефрон: 1 - гломерулна капсула; 2 - тубула на нефрона; 3 - събирателен канал. Кръвоносни съдове на нефрона: а - аферентна артерия; b - еферентна артерия; в - тръбни капиляри; d - вена на нефрона.
При различни патологични процеси настъпва обратимо или необратимо увреждане на нефроните, в резултат на което някои от тях могат да спрат да изпълняват функциите си. В резултат на това има промяна в производството на урина (задържане на токсини и вода, загуба на полезни веществапрез бъбреците и други синдроми).
Концепцията за гломерулна филтрация
Процесът на образуване на урина се състои от няколко етапа. На всеки от етапите може да възникне неуспех, водещ до нарушаване на функцията на целия орган. Първата стъпка в образуването на урина се нарича гломерулна филтрация.
Осъществява се от бъбречното телце. Състои се от мрежа от малки артерии, образувани под формата на гломерул, заобиколен от двуслойна капсула. Вътрешният лист на капсулата приляга плътно към стените на артериите, образувайки бъбречната мембрана (гломерулен филтър, от латински glomerulus - гломерул).
Състои се от следните елементи:
- ендотелни клетки (вътрешна "лигавица" на артериите);
- епителни клетки-капсули, образуващи вътрешния му лист;
- слой от съединителна тъкан (базална мембрана).
Чрез бъбречната мембрана се отделят вода и различни вещества и от нейното състояние зависи колко пълноценно бъбреците изпълняват своята функция.
Големи (протеинови) молекули и клетъчни елементи на кръвта не преминават през бъбречната мембрана. При някои заболявания те все още могат да преминат през него поради повишената му пропускливост и да попаднат в урината.
Разтворът на йони и малки молекули във филтрираната течност се нарича първична урина. Съдържанието на вещества в състава му е много ниско. Подобно е на плазмата, от която протеинът е отстранен. Бъбреците филтрират от 150 до 190 литра първична урина за един ден. В процеса на по-нататъшна трансформация на първичната урина в тубулите на нефрона, крайният й обем намалява около 100 пъти до 1,5 литра (вторична урина).
Тубулна секреция и реабсорбция - процесите на образуване на вторична урина
Поради факта, че голямо количество вода и вещества, необходими за тялото, влизат в първичната урина по време на пасивна тубулна филтрация, би било биологично непрактично да се отстрани от тялото непроменено. В допълнение, някои токсични вещества се образуват в доста големи количества и тяхното отделяне трябва да бъде по-интензивно. Следователно първичната урина, преминавайки през системата от тубули, претърпява трансформация чрез секреция и реабсорбция.
На фиг. 2 показва модели на тубулна реабсорбция и секреция.
Тубулна реабсорбция (1). Това е процес, в резултат на който водата, както и необходимите вещества, чрез работата на ензимни системи, йонообменни механизми и ендоцитоза, се „вземат” от първичната урина и се връщат обратно в кръвния поток. Това е възможно поради факта, че тубулите на нефрона са плътно преплетени с капиляри.
Тубулната секреция (2) е обратният процес на реабсорбцията. Това е отстраняването на различни вещества с помощта на специални механизми. Епителните клетки активно, противно на осмотичния градиент, "изтеглят" определени вещества от съдовото легло и ги секретират в лумена на тубулите.
В резултат на тези процеси в урината се наблюдава повишаване на концентрацията на вредни вещества, чието отделяне е необходимо, в сравнение с концентрацията им в плазмата (например амоняк, метаболити на лекарства). Освен това предотвратява загубата на вода и хранителни вещества (например глюкоза).
Някои вещества са индиферентни към процесите на секреция и реабсорбция, тяхното съдържание в урината е пропорционално на това в кръвта (един пример е инсулинът). Корелирането на концентрацията на такова вещество в урината и кръвта ни позволява да заключим колко добре или лошо се извършва гломерулната филтрация.
Скорост на гломерулна филтрация: клинично значение, принцип на определяне
Скоростта на гломерулна филтрация (GFR) е показател, който е основното количествено отражение на процеса на образуване на първична урина. За да разберете какви промени отразяват колебанията в този показател, е важно да знаете от какво зависи GFR.
Влияят се от следните фактори:
- Обемът на кръвта, преминаваща през съдовете на бъбреците за определен период от време.
- Филтрационното налягане е разликата между налягането в артериите на бъбрека и налягането на филтрираната първична урина в капсулата и тубулите на нефрона.
- Филтрираща повърхност - общата площ на капилярите, които участват във филтрацията.
- Броят на функциониращите нефрони.
Първите 3 фактора са относително променливи и се регулират от локални и общи неврохуморални механизми. Последният фактор - броят на функциониращите нефрони - е доста постоянен и именно той най-силно влияе върху промяната (намаляването) на скоростта на гломерулната филтрация. Следователно, в клинична практика GFR най-често се изследва за определяне на стадия на хронична бъбречна недостатъчност (развива се точно поради загубата на нефрони поради различни патологични процеси).
ЗАТЛЪСТЯВАНЕ И МЕТАБОЛИЗЪМ 1"2009г
Концентрационната функция на бъбреците при първичен хиперпаратироидизъм
Първичният хиперпаратироидизъм (pHPT) е заболяване с много клинични прояви: остеопороза и повишен риск от фрактури, образуване на камъни в бъбреците, влошаване на бъбречната функция, пептична язва на стомаха и дванадесетопръстника, мускулна слабост, умора, всички от които са пряка последица от повишаване на нивото на паратироидния хормон (PTH) и хиперкалцемия. Един интересен аспект на това заболяване е полиурията и полидипсията. Понастоящем патогенезата на тези явления е малко проучена и дори наличните клинични описания на тяхната тежест са само разпръснати данни, открити в някои публикации. Целта на този обзор е да обобщи наличните клинични данни и да изясни механизмите на развитие на симптомите.
Полиурията често придружава pHPT, но тежката полиурия и дехидратацията са редки, обикновено само при тежко заболяване, придружено от високи нива на ПТХ и калций. В допълнение, концентрационната функция на бъбреците почти винаги се възстановява след радикално хирургично лечение. Ето защо повечето клиницисти третират полиурията с pGPT някак пренебрежително. Въпреки това, поради факта, че pHPT сега се диагностицира все по-често, много пациенти имат лека форма на заболяването, не всички пациенти се нуждаят от хирургично лечение и може би консервативно управление и наблюдение, вниманието към нарушената бъбречна концентрационна функция трябва да се увеличи. В проучване за предиктори на смърт при pGPT, увредената бъбречна концентрираща функция е един от важните фактори, заедно с по-напреднала възраст, мъжки пол, намалена гломерулна филтрация, наличие на сърдечно-съдово заболяване, захарен диабет и голям обем резециран тумор. Повишаването на 24-часовия осмолалитет на урината, измерен с натоварване с питресин, минирин или по време на тест със суха диета, с 1 mosmol/l намалява риска от смърт с 0,11%. В същото време рискът от смърт при пациенти, подложени на pHPT, във всеки случай е по-висок от популацията, дори при запазена бъбречна концентрационна функция.
Според изследването на G. Hedback et al.
А.В. Беляева, Н.Г. Мокришева, Л.Я. Рожинская
Федерална държавна институция Център за ендокринологични изследвания, Москва (директор - академик на Руската академия на науките и Руската академия на медицинските науки, проф. I.I. Дедов)
централна функция на бъбреците при pGPT, осмоларитетът на урината на фона на стимулационни тестове при пациенти с pGPT е 636+160 mosmol/l. След аденомектомия в рамките на една седмица 59 от 63 пациенти са имали значително повишаване на осмоларитета на урината със 143+114 mosmol/l, средно с 28%. При останалите пациенти концентрационната функция на бъбреците не се променя или леко се влошава. Анализът на дългосрочния ефект (3-5 години) на аденомектомията в същото проучване показа, че през това време осмотичността на урината остава във възходяща тенденция, подобрение в сравнение с предоперативните показатели се наблюдава при 33 от 35 пациенти с 202+ 132 mosmol/l, тогава има средно 37%. Основен недостатък на изследването е неговият ретроспективен характер, липсата на рандомизация при формирането на извадката и липсата на контролна група.
Според изследователите основното постижение на тяхната работа е доказателството, че след хирургично лечение се възстановява концентрационната функция на бъбреците. Този резултат потвърждава данните от две подобни изследвания, проведени през 60-те години на миналия век с по-точни и статистически обработени данни. Анализът също така предостави доказателства, че степента на повишаване на осмоларитета на урината зависи от нивото на калций преди операцията и в по-малка степен от възрастта на пациента, наличието на съпътстващо увреждане на сърдечно-съдовата система и тежестта на ежедневните хиперкалциурия. Може да се предположи, че първоначалната тежест на заболяването пряко засяга концентрационната функция на бъбреците. Въпреки това, при пациенти с лека форма на заболяването, въпреки че не са включени в проучването, само 14 души, също има възстановяване на осмоларитета на урината след хирургично лечение и първоначалните показатели като цяло не се различават от основната група. Сред пациентите с непроменен или, противно на очакванията, намален осмолалитет, почти всички са имали уролитиаза и инфекция на пикочните пътища, докато при повечето пациенти с подобно бъбречно увреждане възстановяването на осмолалитета на урината е настъпило напълно. Опитите да се свърже степента на възстановяване на осмоларитета на урината с нивото на креатинина в кръвта, скоростта на гломерулна филтрация, увреждане на костите, нервно-мускулни симптоми са неуспешни. Седем
пациентите, проследявани средно пет години без хирургично лечение, се наблюдава намаляване на осмоларитета на урината с 15±8%, но авторите не посочват динамиката на основното заболяване и състоянието на бъбреците при тези пациенти. В друго изследване на същите автори е установена слаба значима корелация между осмоларитета на урината и обема на отстранения тумор, което индиректно показва, че нарушението на концентрационната функция на бъбреците е отражение на тежестта на заболяването. Интересното е, че повишеният риск от смърт с влошаване на бъбречната концентрираща функция не съответства на леко намаляване на риска от смърт при пациенти с уролитиаза, въз основа на което авторите заключават, че механизмът на увреждане на бъбреците, водещ до намаляване на концентрационната функция при pGPT и образуването на камъни може да е различно.
Обратимостта на нарушената концентрационна функция на бъбреците също е показана в друга работа. Авторите отбелязват при пациент с pGPT плазмена хиперосмоларност, полиурия, изостенурия, както и загуба на K + от бъбреците и повишаване на серумните нива на вазопресин. След аденомектомия всички показатели, с изключение на хиперкалиурията, се нормализираха. В друго клинично описание на два случая на хиперкалцемична нефропатия, свързана с pGPT, пациентите са подложени на бъбречна биопсия. Хистологичното изследване разкрива признаци на хронични възпалителни промени в интерстициума на бъбрека и фокална атрофия и некроза на тубулите, както и фокална склероза на гломерулите. Трябва да се отбележи, че описанието на клиничната картина съответства на тежката форма на pGPT и в двата случая.
В проучване на Jansson S. (през 2004 г.), в което е проведено проучване на 20 пациенти, напротив, е показано, че нито след инжектиране на бифосфонати, нито след хирургично лечение на pGPT, са настъпили промени в осмоларитета на урината . Трябва да се отбележи, че в това проучване осмоларитетът на урината е определен без предварителна стимулация и е извършена рехидратация при тези пациенти, които са се нуждаели от нея преди лечението. Подобен резултат е получен в проучването на van "t Hoff W. и Bicknell E.J., по време на което са изследвани 29 пациенти, които са наблюдавани консервативно средно 2,7 години, и 17 оперирани пациенти. Общо нивото на осмоларитет е измерено в началото и по време на наблюдението на урината в пробата със суха диета и не е открито нарушение на концентрационната функция на бъбреците при никого. Авторите заключават, че най-вероятно нарушението на концентрационната функция на бъбреците е характерно само за много тежки форми на заболяването, които в момента са редки, но не изключват възможността, че в изследването на Marx S. J. et al., осмоларитетът на урината е оценен в проба със суха диета при 40 пациенти с pGPT.18 оперираните пациенти не показват подобрение след месец.
По този начин не е напълно ясно какво определя степента и наличието на първоначалното увреждане и последващото възстановяване на концентрационната функция на бъбреците, какви са механизмите за прогресиране на тубулопатията.
Сега е известно, че симптомът на полиурия е свързан повече с хиперкалциурия, отколкото с хиперкалциемия. От клинични примери е известно, че полиурията може да придружава хиперкалциурия от различен произход. Обратно, при наследствена хипокалциурична хиперкалциемия, свързана с мутация в гена на чувствителния към калций рецептор (CASR), полиурия не се наблюдава. Известно е също, че при здрави хора концентрацията на калций в урината зависи не само от дневния му прием, но и от режима на пиене. Например, калциурията се увеличава значително при ограничаване на водата, тъй като реабсорбцията на вода в събирателните канали на нефрона се увеличава чрез стимулиране на вазопресина. Смята се, че това е причината честотата на уролитиазата, до голяма степен свързана с повишаване на калциурията, да е по-висока в горещи сухи райони.
Нарушаването на концентрационната функция на бъбреците възниква поради директния токсичен ефект на хиперкалцемия и хиперкалциурия върху процесите на тубулна реабсорбция. Получената полиурия може да достигне 3-5 литра на ден и да доведе до дехидратация, загуба на натрий, калий, магнезий и фосфати.
За по-добро разбиране на процесите на конюгиране на транспорта на калций и вода в нефрона е необходимо да се разберат по-задълбочено процесите на реабсорбция на Ca2+. При здрав човек се екскретира по-малко от 2% от филтрирания в бъбречните гломерули калций. Очевидно реабсорбцията на калций е много интензивна. Реабсорбцията на Ca2+ се осъществява в почти всички части на нефрона и се регулира от SLBP, PTH, калцитонин и калцитриол. Струва си да се отбележи, че регулацията е много фино настроена, тъй като дори малка разлика между калций, постъпващ в тялото и отделен от бъбреците, може да доведе до подчертан дисбаланс на калций и калций, ако продължи много дни.
Локалното регулиране на екскрецията на Ca2+ и конюгирането на екскрецията на Ca2+ с реабсорбцията на Na+ и вода се осигурява от SLBP. SLBP се експресира в много части на нефрона. Това са апикалната мембрана на проксималния извит тубул и базолатералната мембрана на кортикалния и медуларния дистален ректален тубул на бримката на Хенле и дисталния извит тубул, както и някои клетки на кортикалните събирателни канали и, разбира се, апикална мембрана на събирателния канал на вътрешната зона на медулата. Има доказателства, че SLBE влияе върху функционирането на преносителите на Ca2+/Mg2+ във всички региони.
Приблизително 70% от филтрирания Ca се реабсорбира в проксималните извити и проксималните ректусни тубули. Този процес е изоосмотичен, т.е. Ca2+, Na+ и водата се реабсорбират паралелно. Движещата сила зад реабсорбцията е в началото (т.е.
ЗАТЛЪСТЯВАНЕ И МЕТАБОЛИЗЪМ 1"2009г
ЗАТЛЪСТЯВАНЕ И МЕТАБОЛИЗЪМ 1"2009г
в по-проксималната част) концентрация, след това електрохимичен градиент. Приблизително 1/5 Ca се реабсорбира трансепително. По принцип проксималният нефрон, доколкото е известно, не участва във връзката между обмена на Ca2+ и вода.
Примка на Хенле. Тънките низходящи и възходящи сегменти на бримката на Хенле са практически непропускливи за Ca2+ и изключително пропускливи за Ca+ и вода. Въпреки това, Ca2+ е пропусклив за дисталния ректален тубул на примката на Henle, който съдържа редица калциеви канали и CaK2C1 котранспортера. В това последно място около 20% от филтрирания калций се реабсорбира.
Повечето от експерименталните данни показват, че калциевата реабсорбция е пасивна под действието на положителен електрохимичен градиент в лумена на тубула. Основният транспортен механизъм е параепителният път. Известно е, че тесните контакти на клетките на тази област (т.е. междуклетъчната зона) включват протеина парацелин-1 (parasell-1, PCK-1), който вероятно упражнява основния контрол върху пасивната реабсорбция на Ca ( и в същото време Mg2+). Този видтранспортът зависи от транспорта на Ка+, участващ в създаването на трансепителния електрохимичен градиент. Нарушаването на транспорта на Ca +, например, Ca + помпата, която отстранява Ca + от клетката от базолатералната страна, влияе директно върху реабсорбцията на Ca2 +. Парацелуларният транспорт на Ca2+ обаче не влияе върху реабсорбцията на Ca+. Това се потвърждава от идентифицираното наследствено заболяване, свързано с хомозиготна мутация на PCNK-1 и водещо до повишена бъбречна загуба на Ca2+ и Mg2+, но с интактна реабсорбция на Ca+ и C1- в този сегмент (първична хипомагнезиемия).
Въпреки това има доказателства за активен транспорт на Ca2+ в дисталния ректус тубул на кортикалните (къси) бримки на Henle. Активният транспорт е трансепителен. Ca2+ от страната на апикалната мембрана навлиза в клетката под действието на силен концентрационен градиент, а от базолатералната страна се отстранява от клетката с помощта на Ca+/Ca2+ обменника. Смята се, че дейността на този конкретен обменник се регулира от PTH, въпреки че механизмите на регулиране не са напълно ясни.
В резултат на калциевия транспорт и в зависимост от серумната концентрация на Са2+ се създава определена концентрация на Са2+ в интерстициалното пространство на базолатералната страна на тубула. Известно е, че SLBP са разположени върху базолатералната мембрана на епитела на дисталния ректален тубул. Взаимодействието с Ca2+ йони има инхибиторен ефект върху CaK2C1 котранспортера на апикалната мембрана, K+ NROM каналите на апикалната мембрана, които осигуряват рециркулация на K+, и върху 3Ka+/2K+ обменника на базолатералната мембрана. Най-вероятно ефектът от активирането на SLBP се дължи на намаляване на производството на cAMP и увеличаване на разграждането му, което е причината за инхибирането на K+ каналите. Има доказателства, че стимулирането на SLBE води и до увеличаване на производството на други молекули (например 20-HETE), които допълнително инактивират
K+ канали. В резултат на тези процеси се намалява рециркулацията на K+ и в съответствие с това намалява транспорта на Na+, C1-, а след тях и Ca2+, Mg2+. Известно е, че активиращите мутации в гена SLAD са причина за синдрома на Bartter тип V, при който наред с хипокалиемичната метаболитна алкалоза има загуба на Ка от бъбреците и компенсаторна хиперренинемия и хипералдестеронизъм. Вероятно ролята на SLAD в този сегмент при физиологични условия е реакцията на относителна хиперкалцемия. По-малката реабсорбция на натрий намалява трансепителния електрохимичен градиент (положителен в лумена, отрицателен от базолатералната страна), който е основната движеща сила на Ca2+ реабсорбцията в този сегмент. По този начин се намалява реабсорбцията на калций. Описаният механизъм е донякъде подобен на действието на бримковите диуретици, тъй като намаляването на реабсорбцията на Ca + в дисталния ректален тубул намалява осмотичния градиент, който е в основата на функционирането на противоточната система. Въпреки това, тежестта на инхибиторния ефект, упражняван от SLBP върху горните вектори, не е известна.
Дистален извит тубул и съединителна тръба (свързващ тубул). В дисталната част на нефрона, състояща се от дисталния извит тубул и свързваща тръба, около 15% от филтрирания Ca2+ се реабсорбира. В тези сегменти реабсорбцията се осъществява чрез активен трансцелуларен транспорт срещу съществуващия електрохимичен градиент. Точното местоположение на зоните, в които се осъществява трафикът, остава спорно. Известно е, че по-голямата част от калциевите канали и транспортери са концентрирани в дисталната трета на дисталния извит тубул и в свързващата тръба. Точните механизми на регулиране на тези преносители са неизвестни. Има доказателства, че транспортната активност на Са2+ се контролира от ПТХ, калцитонин и калцитриол. Например, PTH стимулира Ca+/Ca2+ обменника, разположен върху базолатералната мембрана, както и в дисталния ректус тубул на примката на Henle, но са предложени много други механизми за PTH стимулиране на Ca2+ реабсорбция. Също така няма доказателства, че концентрацията на Ca2+ оказва влияние върху водния транспорт в тези сегменти.
събирателни тръби. Събирателните канали са отговорни за реабсорбцията на около 3% калций. Преносът на Ca2+, както и в дисталните тубули, протича срещу електрохимичен градиент и е активен. Известно е, че Ca2+ носителите са разположени върху основните клетки (в този раздел фигурират интеркаларните, отговорни за киселинно-алкалния баланс). Чрез калциевите канали Ca2+ от лумена на тубула навлиза в клетката на тубуларния епител, след което с помощта на редица вътреклетъчни транспортни протеини Ca2+ се придвижва към базолатералната повърхност, след което се отстранява в интерстициалното пространство с помощта на калциеви помпи. При изследване на транспорта на Ca2+ в събирателните канали на вътрешната зона на медулата при плъхове, методът на микроперфузия установява
но тази транспортна активност зависи от трансепителния концентрационен градиент на Ca2+. Според други проучвания, транспортната активност не се е променила след тиреопаратиреоидектомия, т.е. не зависи от нивото на ПТХ и калцитонин, а иРНК на ПТХ рецептора и пептида, свързан с ПТХ, не се открива в епитела на събирателните канали. .
В проучване на Sands J. et al. проведено върху плъхове, беше показано, че събирателните канали на вътрешната зона на медулата съдържат механизъм, който отслабва действието на вазопресина с повишаване на интралуминалната концентрация на Ca2+. Повишаването на интралуминалната концентрация на Ca2+ от 1 до 5 mmol/l в присъствието на вазопресин бързо (в рамките на 10 минути) и значително намалява пропускливостта на стената на тубула за вода с 30%. Този ефект се повтаря с използването на CASR агонист неомицин и се елиминира частично след измиване на разтвора, който перфузира тубула. Използването на специфични антитела в същото проучване показа, че при хора и плъхове CASRs са разположени главно в дисталната трета на събирателните канали на вътрешната зона на медулата върху апикалната мембрана, както и във водните канали, аквапорин-2. И че, очевидно, сигналната трансдукция се дължи на протеин киназа С, която също присъства в тези клетки и е известен CASR сигнален медиатор.
В друго проучване при плъхове е показано, че пиковият бъбречен концентрационен капацитет при хиперкалциемия е намален с около 20% в сравнение с контролите чрез отслабване на действието на вазопресин, дори след коригиране на повишеното производство на простагландин в бъбреците и намаления медуларен осмотичен градиент.
В допълнение към механизмите, описани по-горе, при плъхове с PTH-индуцирана хиперкалциемия се наблюдава повишаване на експресията на CASR гена и намаляване на експресията на гени на много Na+ носители от проксималния извит тубул до събирателните канали, което е придружено от намаляване на концентрационната способност на бъбреците, хипернатриурия, хиперкалциурия, хиперфосфатурия. Разкритият ефект зависи от приложената доза ПТХ. При симулиране на тежък хиперпаратиреоидизъм е изразено потискането на експресията на гени носители на Na +, което очевидно играе роля в развитието на нарушение на концентрационната функция на бъбреците, натриурия и фосфатурия. С въвеждането на по-ниска доза ПТХ, концентрацията на урината се намалява, но няма полиурия, натриуреза и намаляване на гломерулната филтрация, а намаление на експресията се отбелязва само за гените на някои носители. В друго проучване беше показано, че ПТХ може също да намали коефициента на гломерулна ултрафилтрация и следователно скоростта на гломерулна филтрация. В проучване на Wang W., et al, където хиперкалциемия е индуцирана при плъхове чрез предозиране на витамин D, не е установено намаляване на експресията на Na+ транспортерни гени, така че е възможно този ефект да се дължи на действието на PTH , а не хиперкалцемия per se.
Методът, описан по-горе, е конюгирането на хомеостазата на калций и вода на ниво
бъбреци. Неговата физиологична необходимост е да се предотврати появата на прекомерна концентрация на калций в тубулната течност и урината. Когато е необходима повишена бъбречна екскреция на калций в резултат на прекомерен прием на калций, малки колебания в концентрацията на калций в перитубулната интерстициална течност водят до медиирано от CASR намаляване на транспорта на NaCl и Ca2+ в дисталния ректус тубул на примката на Henle. Тубулната течност с повишено количество NaCl, следователно вода и Са2+ достига до събирателните каналчета на вътрешната зона на медулата, където при условия на максимално стимулиране с вазопресин все още има възможност за ново повишаване на концентрацията на калций и образуването на калциево-оксалатни или фосфатни пикочни камъни. Втори механизъм помага да се избегне това, който намалява ефективността на вазопресина върху реабсорбцията на вода и предотвратява повторното повишаване на концентрацията на калций. Вариациите в броя на преносителите на Ka+ и CASR също допринасят за намаляване на концентрационния капацитет на бъбреците. По този начин във всички части на нефрона, особено тези, свързани с активна реабсорбция на вода, концентрацията на Ca2+ се поддържа на ниво, което предотвратява образуването на камъни.
В условията на патологична хиперкалциурия ефектът на Ca2+ върху SLBP на нивото на бримката на Henle увеличава обема на интратубулната течност, а на нивото на събирателните канали се допълва от действителното развитие на бъбречната форма на безвкусен диабет, което е свързано с бъбречна резистентност към вазопресин.
Осъществяването на горните механизми при условия на pGPT води до дехидратация на организма като цяло. При леки случаи дехидратацията може да се компенсира с повишен прием на течности и дори да остане незабелязана от пациента. Въпреки това, в тежки случаи на висока хиперкалциемия (общ серумен Ca е над 3,5 mmol/l), дехидратацията на тялото става важен патофизиологичен компонент на тежкото състояние на пациента. Общата дехидратация също може да допринесе за повръщане и глад поради загуба на апетит и обща летаргия. При хиперкалциемична криза дехидратацията може да достигне такива стойности, че поради намаляване на скоростта на гломерулната филтрация полиуричният стадий може да се превърне в олигоурен. Ето защо лечението на висока хиперкалциемия, чиято основна цел е да намали нивото на калций в кръвта възможно най-бързо, трябва да започне с попълване на обема на циркулиращата кръв. Само след рехидратация на тялото и възстановяване на диурезата, ако тя е намалена, се препоръчва форсирана диуреза, тъй като увеличаването на натриурията увеличава калциурията и специфична хипокалцемична терапия.
Един от най-интригуващите аспекти на обсъждания проблем е, че тежестта на наблюдаваното увреждане на концентрационната функция на бъбреците варира значително в рамките на приблизително същата хиперкалциурия и хиперкалциемия в рамките на pGPT. Едно от възможните обяснения на този феномен
ЗАТЛЪСТЯВАНЕ И МЕТАБОЛИЗЪМ 1"2009г
ЗАТЛЪСТЯВАНЕ И МЕТАБОЛИЗЪМ 1"2009г
Промяната може да бъде полиморфизъм на CASR гена, свързан с малко по-висока или малко по-ниска чувствителност на рецептора към Ca2+. Понастоящем са идентифицирани няколко полиморфни варианта на CASR гена, които се наблюдават при здрави хора и при пациенти с уролитиаза. По отношение на един от хаплотиповете беше показано, че присъствието му в хомохетерозиготна позиция корелира с концентрацията на Ca2+ в кръвния серум, докато другият хаплотип е свързан с повишен риск от уролитиаза. Тези изследвания ясно демонстрират, че калциевият метаболизъм на отделния организъм зависи от полиморфния вариант на CASR гена. Следователно тежестта на реакцията на бъбреците към хиперкалциемия/хиперкалциурия може също да зависи от това.
Обобщавайки прегледа, можем да кажем, че влошаването на концентрационната функция на бъбреците е несъмнен симптом на хиперкалциурия / хиперкалцемия. Може също да има пряк принос към развитието
Синдромът допринася за повишени нива на ПТХ. Въпреки факта, че тежестта на намаляването на концентрационната функция на бъбреците може да варира значително, дехидратацията винаги настъпва със значително повишаване на нивото на калций в кръвта и урината. Бъбречните механизми на това патологично състояние се осъществяват главно чрез активирането на CASR от Ca2+ йони в различни части на нефрона. Предимно дисталния ректален тубул на бримката на Хенле и събирателните канали. Физиологичният смисъл на което е да се предотврати прекомерното повишаване на концентрацията на Ca2 + в тубулната течност и да се намали рискът от образуване на камъни. В статията се разглеждат механизмите на обратимо бъбречно увреждане при pHPT, които са пряко следствие от характерни метаболитни промени. В редки случаи тубулопатията персистира дори след радикално лечение на pHPT. Защо възникват дълбоки увреждания, както и причините за такъв различен индивидуален отговор на хиперкалциемия/хиперкалциурия при pHPT, остава да бъдат изяснени.
Литература
1. Bengele H, Alexander E, Lechene C. Пренос на калций и магнезий по вътрешния медуларен събирателен канал на плъх. Am J Physiol Бъбречна течност Електролит Physiol. - 1980 - 239 (1) - стр.24-9.
2. Blanchard A, Jeunemaitre X, Coudol P, et al. Парацелин-1 е критичен за реабсорбцията на магнезий и калций в човешкия дебел възходящ крайник на Henle. Kidney Int - 2001 - 59(6) - pp. 2206-2215.
3. Blaustein M, Lederer W. Натриев/калциев обмен: неговите физиологични последици. Physiol Rev. - 1999 - 79(3) - стр. 763-854.
4. Bourdeau J, Burg M. Ефект на ПТХ върху калциевия транспорт през кортикалния дебел възходящ крайник на бримката на Хенле Am. J. Physiol.- 1980 - 239 (2) - стр. 121-6.
5. Edvall CA. Бъбречна функция при хиперпаратироидизъм. Acta Chir Scand. -1958 -229 (Suppl) - pp. 5-56.
6. Egbuna O, Brown E Хиперкалциемични и хипокалциемични състояния, дължащи се на мутации на калциево-чувствителни рецептори. Най-добри практики Res Clin Rheumatol. - 2008-22(1)-стр. 129-48.
7. Ellis G, Spirtos G, Polsky F. Първичен хиперпаратироидизъм и съпътстващ нефрогенен безвкусен диабет: бърза постоперативна корекция. South Med.J-1991-84(8)-pp. 1019-22.
8. Fenton R, Knepper M. Модели на мишки и механизмът за концентриране на урината през новото хилядолетие. Physiol Rev. - 2007 - 87(4) - стр. 1083-1112.
9. Hebert S, Desir G, Giebisch G, Wang W. Молекулярно разнообразие и регулиране на бъбречните калиеви канали. физиол. Rev. - 2005 - 85(1) -стр. 319-371.
10. Hedback G, Abrahamsson K, Oden A. Подобряването на капацитета на бъбречната концентрация след операция за първичен хиперпаратироидизъм. Eur J Clin Invest - 2001 -31 - pp. 1048-53.
11. Hedback G, Oden A. Анализ на рисковия фактор за смърт при първичен хиперпаратироидизъм. Eur J Clin Invest - 1998 - 28 (12) - стр. 1011-1018.
12. Hedback G, Oden A. Повишеният риск от смърт от първичен хиперпаратироидизъм, актуализация. Eur J Clin Invest - 1998 - 28(4) - стр. 271-6.
13. Hellstrom J, Ivemark B. Първичен хиперпаратироидизъм, клинични и структурни находки в 138 случая. Acta Chir Scand. - 1962 - 294 (Suppl) - pp. 7-60.
14. Hoenderop J, Nilius B, Bindels R. Абсорбция на калций през епитела. физиол. Rev. - 2005 - 85(1) - стр. 373-422.
15. van "t Hoff W, Bicknell E. Бъбречна тубулна функция при хиперпаратироидизъм. Postgraduate Med J. - 1989 - 65 (769) - стр. 811-3.
16. Jansson S, Morgan E. Биохимични ефекти от лечение с бифосфонат и хирургия при пациенти с първичен хиперпаратироидизъм. World J Surg. -
2004 - 28(12) - стр. 1293-97.
17. Kashitani T, Makino H, Nagake Y et al. Два случая на хиперкалцемична нефропатия, свързана с първичен хиперпаратироидизъм. Nippon Jinzo Gakkai Shi. - 1993 -35(10) - стр. 1189-94.
18 Kausalya P, Amasheh S, et al. Свързаните със заболяването мутации засягат вътреклетъчния трафик и парацелуларната Mg2+ транспортна функция на клаудин-16. J Clin Invest. -2006 - 116(4) - стр. 878-891.
19. Kukora J, ZeigerM, et al. Изявлението за позиция на Американската асоциация на клиничните ендокринолози и Американската асоциация на ендокринните хирурзи относно
диагностика и лечение на първичен хиперпаратироидизъм. Ендокр. практика-
2005 - 11 (1) - стр. 49-54.
20. Kushner D Калцият и бъбреците. Am J Чисто хранене. -1986-4(5)-стр. 561-679.
21. Lee K, Brown D, et al. Локализация на мРНК на пептидния рецептор на паратироидния хормон/паратироидния хормон в бъбреците. Am J Physiol Бъбречна течност Електролит Physiol. - 1996 - 270 - стр. 186-91
22. Леви М, Питърсън Л, Берл Т. Механизъм на концентриращ дефект при хиперкалцемия. Роля на полидипсията и простагландините. Kidney Int. - 1983 - 23 - стр.489-97.
23. Magaldi A, van Baak A, Rocha A. Пренос на калций през вътрешен медуларен събирателен канал на плъх, перфузиран in vitro. Am J Physiol Бъбречна течност Електролит Physiol. -1989 - 257 - стр.738-45.
24. Marx S, Attie M. Максимална способност за концентриране на урината: фамилна хипокалциурична хиперкалцемия срещу типичен първичен хиперпаратироидизъм. J Clin Endocrinol Metab. -1981-52(4)-стр.736-40.
25. Poujeol P, Bidet M, Tauc M. Пренос на калций в дисталните клетки на заек. Kidney Int. -1995-48-стр. 1102-1110.
26 Sands J, Naruse M, et al. Апикален екстрацелуларен калциев/поливалентен катион-чувствителен рецептор регулира водната пропускливост, предизвикана от вазопресин във вътрешния медуларен събирателен канал на бъбрека на плъх. J Clin Invest. - 1997 - 99 (6) - стр.1399-1405.
27. Schor N, Ichikawa I, Brenner B. Механизми на действие на различни хормони и вазоактивни вещества върху гломерулната ултрафилтрация при плъхове. Kidney Int. - 1981-20-стр. 442-51.
28 Scillitani A, Guarnieri V, Battista C, et al. Първичният хиперперетиреоидизъм и наличието на камъни в бъбреците са свързани с различни хаплотипове на калциево-чувствителния рецептор J Clin Endocrinol Metab. - 2007 - 92(1) - стр. 277-83.
29 Scillitani A, Guarnieri V, De Geronimo S, et al. Йонизираният в кръвта калций се свързва с клъстерни полиморфизми в карбоксилната крайна опашка на калций-чувствителния рецептор. J Clin Endocrinol Metab. - 2004 - 89 - стр.5634-38.
30. Vargas-Poussou R, Huang C, et al. Функционална характеристика на мутация на калций-чувствителен рецептор при тежка автозомно-доминантна хипокалциемия с подобен на Bartter синдром. J Am Soc Nephrol. - 2002 - 13 -стр. 2259-2266.
31. Vezzoli G, Tanini A, Ferrucci L, et al. Влияние на калциево-чувствителния рецепторен ген върху екскрецията на калций в урината при пациенти, образуващи камъни. J Am Soc Nephrol. -2002-13-стр. 2517-23.
32. Wang W, Kwon T, et al. Намалена експресия на Na-K-2Cl котранспортер в медуларен TAL при индуцирана от витамин D хиперкалцемия при плъхове. Am J Physiol Renal Physiol. - 2002 - 282 - стр.34-44.
33. Wang W, Lu M, Hebert S. Метаболитите на цитохром P-450 медиират екстрацелуларното Ca2+-индуцирано инхибиране на апикалните K+ канали в TAL. Am J Physiol Cell Physiol - 1996 - 271-pp. 103-111.
34. Watanabe S, Fukumoto S, et al. Асоциация между активиращите мутации на калций-чувствителния рецептор и синдрома на Bartter Lancet - 2002 - 360 - стр. 692-694.
35. Weidong W, Chunling L, et al. Намалена експресия на бъбречни Na+ транспортери при плъхове с PTH-индуцирана хиперкалцемия. Am J Physiol Renal Physiol. - 2004 -286 - стр.534-45.
9588 0
Регулиране на водното съдържание в организма
Ефективно функциониращите бъбреци поддържат нормален обем и течен състав в тялото, дори при значителни колебания в диетата, екстраренални загуби на вода и разтворени вещества. Водно-електролитният баланс се постига чрез отделяне на урина с определен обем и състав, което се осигурява чрез гломерулна плазмена ултрафилтрация в комбинация с последваща тубулна реабсорбция и секреция.Отделената крайна урина представлява само малка част от гломерулния ултрафилтрат, променен при преминаването към нефрона. Капилярите на гломерулите свободно преминават вода и разтворени вещества с ниско молекулно тегло, като същевременно задържат формирани елементи и макромолекули. Стената на гломерулния капиляр функционира като бариера по отношение на макромолекулите, като ги "подбира" според техния размер, форма и заряд.
Промяната на гломерулния филтрат по време на преминаването му през тубулите се извършва чрез транспортиране на определени вещества, както активни (в лумена на тубулите или извън лумена), така и пасивно. Последното се дължи на осмотичен и електрохимичен баланс и различна пропускателна способност на отделните сегменти на нефрона.
Системата за транспортиране на йони в бъбречните епителни клетки е основно същата като функцията на всички други епителни клетки. Въпреки това, бъбречната транспортна система осигурява общото съдържание на вода, соли и киселинно-алкална хомеостаза в тялото, докато локалните процеси, протичащи в други епителни клетки, регулират само определени „фрагменти“ на водно-солевия метаболизъм, например обем и абсорбция на течности метаболитни продукти..
За да може бъбрекът ефективно да регулира баланса на водата и разтворените вещества, гломерулният филтрат трябва да има подходящ обем. Бъбречният кръвоток е 20-30% от сърдечния дебит. От общия бъбречен плазмен поток, 92% от плазмата преминава през функциониращата отделителна тъкан и се определя като ефективен бъбречен плазмен поток (ERF). Скоростта на гломерулна филтрация (GFR) обикновено е 1/5 от GFR, което води до филтрационна фракция от 0,2.
Скоростта на ултрафилтрация през гломерулните капиляри, GFR, се определя от същите фактори, които определят трансмуралното движение на течността в други капилярни мрежи на тялото, а именно транскапилярни градиенти на хидравлично и осмотично налягане и пропускливост на капилярната стена. Механизмът на бъбречната авторегулация позволява на бъбрека да поддържа относително постоянен кръвен поток в присъствието на променящо се налягане, както на системната артериална, така и на бъбречната перфузия.
Този механизъм изглежда се медиира в нефроните от тубулно-гломеруларен обратна връзкапрез macula densa (областта в началото на дисталния тубул, в съседство с гломерула), както и адукторни и еферентни артериоли. Намаляването на артериоларното съпротивление в аддукторните артериоли, като същевременно се поддържа на стабилно ниво в еферентните артериоли, позволява поддържане на хидродинамичното налягане в гломерула, въпреки спада на системното и бъбречното артериално налягане.
Реабсорбцията на вода, както и реабсорбцията и секрецията на разтворени вещества по време на преминаването на филтрата през нефрона, обикновено служи за поддържане на хомеостазата на течностите в тялото. В здрав, нерастящ организъм приемът и екскрецията на вода и разтворени вещества са равни и по този начин хидройонният баланс е нулев. Механизмите на регулиране на бъбречната функция могат да се променят под влияние на различни заболявания, както системни, така и бъбречни, както и под въздействието на голямо разнообразие от лекарства, като вазопресори и вазодилататори, нестероидни противовъзпалителни средства, диуретици и антибиотици. Бъбречната дисфункция в постоперативния период най-често се проявява чрез хипоксия и намалена бъбречна перфузия.
Оценка на бъбречната функция
Оценката на бъбречната функция започва с подробна анамнеза и физикален преглед на пациента, последвани от лабораторни изследвания за определяне на скоростта на гломерулна филтрация и функцията на бъбречните тубули. Сериозни нарушения на отделителната и концентрационната способност на бъбреците понякога са очевидни от анамнезата.Изследването на уринарния седимент може да разкрие директни признаци на увреждане на гломерулите или бъбречния паренхим. Определянето на серумните електролити, калций и фосфор е ценен метод за скрининг, характеризиращ тубулните нарушения, докато концентрацията на креатинин е основният показател за GFR.
Обем на урината. Често в голямо разнообразие от клинични ситуации е много важно да се определи дали пациентът отделя достатъчен обем урина. Отговорът на въпроса каква диуреза е адекватна е много труден, тъй като този показател зависи от няколко фактора: водния баланс в организма в момента, натоварването с течности и екстрареналните загуби, както и задължителното натоварване с разтворими вещества.
Пациенти с увредена бъбречна концентрационна способност, като сърповидно-клетъчна анемия (при по-големи деца и възрастни) и пост-обструктивна уропатия, се нуждаят от по-голям минимален обем на урината за отделяне на задължителен разтворен товар, отколкото пациенти с нормална бъбречна концентрационна функция.
Въпреки че определянето на "адекватността" на обема на урината в повечето случаи причинява много трудности, въпреки това винаги е важно поне да се изясни въпросът - дали пациентът има олигурична бъбречна недостатъчност с дадена диуреза или не. Решението на този проблем се основава на познаването на минималния обем урина, необходим за отстраняване на задължителен товар от разтворимо вещество.
Изчислението се основава на 100 метаболизирани калории или 100 ml H2O натоварване, което позволява да се правят изчисления независимо от телесното тегло. Физиологичната нужда от вода се определя удобно за тази цел, като се използва методът на Холидей и Сегар (Таблица 5-1). Нормата от 100 ml / kg / ден е приложима за деца с тегло само до 10 kg. Дете с ТМ 15 кг има нужда от вода от 83 мл/кг/ден, а с ТТ 30 кг е 57 мл/кг/ден.
Таблица 5-1. Физиологични нужди от вода
Минималният обем на урината, необходим за отделяне на задължителен разтворен товар, се изчислява, като се използват следните конвенции и допускания.
1. Задължителното натоварване с разтворени вещества, прието за пациент с исхемична остра бъбречна недостатъчност (ARF), ще бъде по-голямо или по-малко от минималното ендогенно натоварване с разтворими вещества от хипотетично 10-15 my/100 калории метаболизирани (или на 100 ml консумирана вода) .. от 40 mosm на 100 калории, погълнати при нормална диета.4 Приблизително 30 my задължително разтворено вещество на 100 ml калории ще бъде прието от нас като задължително натоварване с разтворено вещество при деца на възраст 2 месеца и по-големи.
2. Концентрационният капацитет на бъбреците се увеличава бързо през 1-вата година от живота и през втората година от живота достига нивото, характерно за по-големите деца (1200-1400 mosm / kg) през втората година от живота. Максималният концентрационен капацитет на бъбреците на доносено дете на възраст от 1 седмица до 2 месеца варира от 600 до 1100 mosm / kg, а на възраст 10-12 месеца е средно малко по-висок от 1000 mosm / kg. Таблица 5-2 представя минималните обеми на урината, които позволяват на пациента да се справи със задължителен товар от разтворени вещества, като по този начин осигурява подходящ физиологичен отговор на бъбречна хипоперфузия.
Таблица 5-2. Минимални обеми на урината, необходими за отделяне на задължителен разтворен товар 
При исхемична остра бъбречна недостатъчност диурезата обикновено е значително намалена. Обемът на урината се изчислява по следната формула:
Обем на урината = Натоварване с разтворено вещество (мое) Концентрация на разтворено вещество (мое)
Исхемична остра бъбречна недостатъчност, като правило, липсва при дете на възраст под 2 месеца с обем на урината> 1,25 ml / час / 100 ml получена течност, както и при по-възрастен пациент с диуреза> 1,0 ml / час / 100 мл. Деца с обем на урината под тези нива съответно се нуждаят от допълнително изследване и оценка за олигурична бъбречна недостатъчност.
Неолигуричната бъбречна недостатъчност е сериозно състояние, което се среща почти толкова често, колкото олигуричната бъбречна недостатъчност и се диагностицира, когато има други ясни признаци на намален GFR при нормална диуреза, най-често повишен серумен креатинин или намален креатининов клирънс.
Скорост на гломерулна филтрация. Скоростта на гломерулна филтрация е най-важната мярка за бъбречната функция в много отношения, тъй като тя отразява количеството плазмен ултрафилтрат, навлизащ в тубулите. Намаляването на GFR е основното функционално увреждане както при остра, така и при хронична бъбречна недостатъчност. Определянето на GFR е необходимо не само за оценка на бъбречната функция като такава, но и за правилен изборантибиотици и други лекарства.
Методът за клирънс на инулина за измерване на GFR има редица недостатъци. Концентрацията на серумната урея не се използва като индикатор за GFR поради големи колебания с хранителния прием на азот.
За оценка на GFR на практика най-широко се използва измерването на концентрацията на серумния креатинин и неговия клирънс. При използването на този метод трябва да се имат предвид редица обстоятелства. Например, консумацията на храни с високо съдържание на протеини (месо, птици, риба) повишава серумния креатинин с 22 mmol/l след 2 часа и увеличава скоростта на отделяне на креатинин със 75% през следващите 3 до 4 часа. Съответно, когато се измерва концентрацията на серумния креатинин и неговия клирънс, тези продукти трябва да бъдат изключени от храната. В допълнение, нивата на серумния креатинин могат да се повишат в резултат на приема на определени лекарства, като триметонрим, който се "конкурира" с креатинина в процеса на тубулна секреция.
Триметоприм, без да повлиява GFR, променя концентрацията на креатинин в серума, което може да причини трудности при оценката на пациент с нарушена нощна функция, тъй като фракцията на креатинина в урината, дължаща се на тубулна секреция, се увеличава, докато GFR пада.
Концентрацията на серумния креатинин на новородено през първата седмица от живота съответства на нивото на майката, а от 2-та седмица до 2 години е средно 35 + 3,5 mmol / l. През този възрастов период концентрацията на серумния креатинин е относително постоянна, тъй като няма големи промени в процента на мускулите в тялото по време на процеса на растеж.
Увеличаването на ендогенното производство на креатинин, което корелира с мускулната маса, върви ръка за ръка с увеличаването на GFR. През първите две години от живота, GFR, изразена в ml/min на единица телесна повърхност, се повишава от 35–45 ml/min/1,73 m2 до ниво за възрастни от 80–170 ml/min/1,73 m2. Нормалните серумни концентрации на креатинин се повишават след 2-годишна възраст с пубертета, докато GFR остава сравнително постоянен за единица телесна повърхност.
Това се дължи на развитието на мускулна маса в процеса на растеж на детето и съответно на увеличаване на производството на креатинин, което е по-бързо от увеличаването на GFR на единица телесно тегло. Таблица 5-3 представя средните нива на плазмения или серумен креатинин при различни възрасти.
Таблица 5-3. Нива, плазмен креатинин в различни възрасти 
Фракционна екскреция (FE) на натрий и бикарбонат. Фракционната екскреция е показател за бъбречната функция, който е важен при оценката на някои клинични състояния и представлява количеството (фракцията) на вещество, филтрирано в бъбреците, което се екскретира в урината. Фракционната екскреция се измерва с помощта на креатининов клирънс, който определя GFR и серумни и уринни концентрации на това вещество.
Филтрираното количество се изчислява чрез умножаване на серумната концентрация по GFR, а екскретираното количество се изчислява чрез умножаване на концентрацията на веществото в урината по обема на урината. Следователно, фракционната екскреция на натрий се изчислява, както следва:

където UNa и UCr са концентрациите на натрий и креатинин в урината, съответно RChl и RGg са техните концентрации в плазмата или серума. Тъй като обемите на урината в числителя и знаменателя са намалени и „напускат“ формулата, фракционната екскреция може да се изчисли въз основа на определянето само на концентрацията на натрий и креатинин в проби от кръв и урина, взети приблизително по едно и също време.
Фракционна екскреция на натрий. FENa обикновено е под 1%, но може да се повиши при повишен прием на сол, адаптиране към хронична бъбречна недостатъчност и прилагане на диуретици. При намаляване на бъбречното перфузионно налягане, което обикновено е характерно за хиповолемия и сърдечна недостатъчност, бъбреците, адаптирайки се към възникналите нарушения, значително увеличават тубулната реабсорбция на натрий и вода, в резултат на което урината се екскретира концентрирана и в малки количества. количества. По този начин, SEN< 1 % является физиологической реакцией на уменьшение реналыюй перфузии. При ишемической ОПН ФЭNa обычно > 2%.
Когато се използва FENa за диференциална диагноза между преренална азотемия и остра бъбречна недостатъчност, получените данни могат да бъдат ненадеждни, ако пациентът е получил диуретици малко преди изследването. Преренална азотемия може да се развие при пациенти с предшестващо хронично бъбречно заболяване с FENa > 1% като адаптация към хронично бъбречно заболяване.
Когато тези пациенти имат хиповолизъм, тогава с него могат да бъдат свързани повишеното ниво на урея и серумен креатинин и високо FENa, FENa, както и други „диагностични показатели“, използвани в диференциалната диагноза на преренална азотемия с исхемична остра бъбречна недостатъчност частично свързана, не е патогномонична нито за единия, нито за другия от тези видове патология. FENa обаче дава много важна информацияако се анализира като част от обща клинична оценка.
Фракционна екскреция на бикарбонат. Бъбречната тубулна ацидоза (RTA) е термин, който определя група от нарушения, при които метаболитната ацидоза е резултат от нарушена реабсорбция на филтриран HCO3 или екскреция на водородни йони, при липса на значително понижение на GFR. Обикновено PTA трябва да бъде включена в списъка на патологиите, диференцирани при пациенти с метаболитна ацидоза, нормална серумна анионна празнина (хиперхлоремична метаболитна ацидоза) и pH на урината над 6,0. При пациенти с проксимална RTA, която се развива поради забавяне на тубулната реабсорбция на HC07, pH на урината може да бъде по-малко от 6,0. когато плазмената концентрация на HCO3 е под прага на бъбречна реабсорбция.
С тип IV PTA (опция дистална форма) метаболитната ацидоза с нормална серумна анионна празнина е свързана с хиперкалиемия и кисела урина (вижте обяснението по-долу). Когато при проксималния тип PTA плазмената концентрация на HCO3 се нормализира чрез адекватно приложение на натриев бикарбонат, съдържанието на HCO3 се увеличава в металния нефрон и урината става силно алкална.При нормална диета целият филтриран HCO3 се реабсорбира и HCO3 PE е 0. pH на урината от 6,2 ppm е по-малко, което показва, че HCO3 в урината е незначителен.
PC02 на урината или разликата между pCO2 на урината и кръвта (U-B pCO2). Дисталният PTA в неговата класическа форма се характеризира с хиперхлоремична метаболитна ацидоза, pH на урината над 6,0, непроменена или намалена серумна концентрация на HCO2 и FE HCO3<5% при нормальном уровне сывороточного HCO3. Причиной классического листального ПТА является неспособность клеток нефрона секретировать Н в просвет канальцев, где при наличии НСО3 образуется угольная кислота (Н2С03).
Забавената дехидратация на H2CO3 в медуларните събирателни канали, бъбречното легенче и пикочния мехур води до повишаване на pCO2, което е характерно за нормалната дистална H+ секреция, когато HCO2 в урината е висок (т.е. pCO2 в урината > 80 mmHg или /U—B pCO2/ > 30 mm Hg). pCO2 в урината се определя след прилагане на еднократна доза натриев бикарбонат (2–3 mmol/kg) или диакарб (17 ± 2 mg/kg). Ако по време на изследването нивото на HCO в серума на пациента е значително намалено, по-добре е да се използва не диакарб, а натриев бикарбонат. pCO2 в урината се оценява само след като pH на урината превиши 7,4 и/или концентрацията на HCO3 е по-висока от 40 mEq/L.
Tin IV PTA (дистален вариант на PTA), свързан с ниско pH на урината (< 6,0) и гиперкалиемией, при котором в дистальных канальцах нарушена секреция как Н+, так и К-, связан с неспособностью почек реабсорбировать натрий, что благоприятствует развитию отрицательного потенциала в просвете канальцев или «вольтаж-зависимого» дефекта.
Тази форма от всички варианти на PTA е най-често срещана както при възрастни, така и при деца. Има и нарушение на бъбречния синтез на амоний. Тъй като амониогенезата се инхибира при хиперкалиемия, това води до намаляване на съдържанието на амоний, който служи като буфер в урината и съответно до намаляване на pH на урината вместо намаляване на H-секрецията (NH3 + H+ = NH4) .
Тип IV PTA е физиологично еквивалентен на дефицит на алдостерон, което може да бъде една от причините за тази патология. При деца този тип PTA е проява на истински хипоалдостеронизъм, но е много по-често при паренхимни бъбречни увреждания, особено при обструктивна уропатия. След елиминирането на обструктивните нарушения, проявите на PTA тип IV намаляват в рамките на няколко седмици или месеци.
К.У. Ашкрафт, Т.М. Държач
Изпратете добрата си работа в базата знания е лесно. Използвайте формата по-долу
Студенти, докторанти, млади учени, които използват базата от знания в обучението и работата си, ще ви бъдат много благодарни.
Хоствано на http://allbest.ru/
Министерство на здравеопазването на Република Беларус
EE "Гродненски държавен медицински университет"
на тема „Функционални тестове за оценка на концентрационната функция на бъбреците“.
Гродно 2012 г
Въведение
Бъбреците са основният орган за поддържане на хомеостазата в организма, което се осигурява от следните функции:
Осигуряване на постоянството на киселинно-алкалния, електролитен състав на кръвта;
Поддържане на обема на кръвта и други течности на вътрешната среда;
Екскреция на крайни продукти от метаболизма и чужди вещества;
Секреция на физиологично активни вещества (ренин, простагландини, еритропоетин, активни форми на витамин D).
Изпълнението на всяка от функциите се осигурява от няколко процеса, които са в основата на дейността на бъбреците: гломерулна филтрация, тубулна реабсорбция и секреция, синтез на нови вещества в структурите на бъбреците.
Осмотичната концентрация и осмотичното разреждане на урината играят важна роля в механизма на образуване на урина и поддържане на осмотичната хомеостаза в организма.
Осмотична концентрация - образуването на урина с по-висока концентрация на осмотично активни вещества, отколкото в кръвната плазма. Осмотично разреждане на урината - отделяне на урина с по-ниска концентрация на осмотично активни вещества, отколкото в кръвната плазма.
Показатели за осмотична концентрация са осмоларитет и осмоларитет. Осмоларност (mOsm / l) - концентрацията на осмотично активни вещества в 1 литър разтвор. Осмотичност (mOsm / kg H2O) - концентрацията на осмотично активни вещества в 1 kg вода (т.е. разтворител).
Факторите, които определят плазмения осмолалитет, са концентрацията на натрий, глюкоза, азотни продукти (главно урея), както и нормално липсващите (т.нар. неизмерени) осмоли - алкохоли, манитол. Плазменият осмолалитет е един от най-стриктно поддържаните физикохимични параметри, имащ коефициент на вариация от 1,67% (за сравнение: коефициентът на вариация за калия е 6,6%) [Yu. В. Наточин, 1993]. Нормалният плазмен осмоларитет е 280-295 mOsm/kg H2O.
Осмотичността на урината се определя главно от електролитите и уреята и е 300-800 mOsm/kg H2O. Но в зависимост от стойностите на приема на течности и извънбъбречните загуби, той може да варира в по-широк диапазон - от 200 до 1200 mOsm / kg H2O.
В процеса на осмотично концентриране на урината в бъбреците участват всички отдели на тубулите, интерстициалната тъкан и съдовете на медулата.
Механизми на осмотична концентрация на урината:
* Проксимален тубул: реабсорбцията на вода и осмотично активни вещества (главно натрий и урея) се извършва в такива пропорции, че осмотичността на тубулната течност остава равна на осмотичността на плазмения ултрафилтрат (280-295 mOsm/kg H2O).
* Низходящ участък на бримката на Хенле (стената е пропусклива за вода, непропусклива за осмотично активни вещества): реабсорбцията на вода продължава в интерстициума по осмотичния градиент. Докато се движите от кортикалния слой по медулата на бъбрека към върховете на пирамидите, количеството на тубулната течност постепенно намалява и нейният осмолалитет се увеличава, достигайки 1200-1500 mOsm / kg H2O в точката на завъртане на низходящата част на примката на Хенле във възходящата част.
* Тънкият възходящ участък на бримката на Хенле (пропусклив за вода): в този участък концентрацията на осмотично активни вещества в тубулната течност е по-висока, отколкото в интерстициума, така че водата навлиза в лумена на този участък по осмотичния градиент от интерстициалната тъкан.
* Дебелият възходящ участък на бримката на Хенле (стената е непропусклива за вода, но пропусклива за натрий, хлор): когато течността се движи през този участък, настъпва активна реабсорбция на натрий и хлор и водата остава в лумена на тубулите , а хипотоничният винаги навлиза в началните секции на дисталната извита тубулна течност (по-малко от 200 mOsm/kg H2O).
* Дистални тубули, събирателни канали: протичащият процес на реабсорбция на вода, осмотично активни вещества (натрий, урея) се регулира от антидиуретичен хормон (ADH).
ADH повишава пропускливостта на стените на дисталните тубули и събирателните канали за вода, повишава реабсорбцията на натрий и хлор в клетките на възходящата дебела бримка на Хенле и повишава пропускливостта на стените на събирателните канали за урея в медула на бъбрека. По този начин, под действието на ADH, се увеличава реабсорбцията на вода от лумена на тубулите в интерстициалната тъкан на бъбреците. В резултат на това се отделя малко урина с високо съдържание на осмотично активни вещества в нея (до 1200 mOsm / kg H2O). При дефицит на ADH пропускливостта на стените на дисталния сегмент на нефрона и събирателните канали за вода намалява, натрият продължава да се абсорбира обратно в интерстициалната тъкан и натрупването на урея в бъбречната медула намалява. Това води до намаляване на реабсорбцията на вода, освобождаване на голямо количество хипоосмоларна урина (около 400 mOsm / kg H2O).
Поддържането на водния баланс в организма се осигурява от регулаторната система, включваща волуморецептори, осморецептори, натриорецептори, нервни и хуморални центрове. При дехидратация на тялото концентрацията на осмотично активни вещества в кръвната плазма се повишава, осморецепторите се възбуждат, секрецията на ADH се увеличава и абсорбцията на вода в тубулите се увеличава. Активирането на волуморецепторите (с увеличаване на водата и натриевите соли в организма) води до намаляване на секрецията на ADH, активиране на натриуретичния хормон, намаляване на секрецията на ренин, ангиотензин и алдостерон. Това води до намаляване на реабсорбцията на натрий, увеличаване на диурезата. В крайна сметка обемът на кръвта и извънклетъчната течност се възстановява.
Оценка на функцията на концентрация
бъбречна хомеостаза осмотична урина
За оценка на концентрационната функция на бъбреците се използват редица методи:
1. Определяне на относителната плътност и осмотичност на урината.
Относителната плътност се определя от количеството на разтворените вещества в урината. Относителната плътност на урината се влияе от естеството на храната, количеството изпита течност, тежестта на екстрареналните загуби, естеството на частиците, разтворени в урината (протеин, захар). Обикновено при нормални условия относителната плътност е 1008-1025 g / l.
Осмотичността на урината е по-строг показател, по-малко зависим от природата на разтворените частици. Осмотичността и относителната плътност са тясно свързани (Таблица 1). Използването на единици за осмотичност дава възможност за сравняване на урина и кръв.
2. Тестът на Зимницки е един от най-простите и достъпни методи за изследване на бъбречната функция. С помощта на теста на Зимницки лекарят определя такива бъбречни функции като способността за концентрация и отделяне на урина. Тестът на Зимницки също дава представа за работата на сърцето.
Какво определя теста на Зимницки?
Анализът на урината според Зимницки позволява на лекаря да определи способността на бъбреците да концентрират урината. Концентрационната способност на бъбреците е естествен регулаторен механизъм, който позволява на тялото да поддържа постоянна течна среда. Така например, с увеличаване на количеството течност в тялото (обилно пиене, течна храна), бъбреците секретират голямо количестворазредена урина урина. Напротив, ако човешкото тяло получава малко вода, бъбреците започват да произвеждат много концентрирана урина и по този начин пестят течност.
Анализът на урината според Зимницки определя плътността на урината - това е показател, който изразява количеството на метаболитните продукти, разтворени в урината (соли, протеини, амоняк и др.). Плътността на урината зависи от количеството консумирана течност, както и от концентрационната способност на бъбреците. Нормалната плътност на урината варира от 1,003 до 1,035. През деня човек консумира неравномерно количество течност, така че плътността на урината в различно времедневни промени: през деня урината е с по-малка плътност поради приема на течности, сутрешната урина, напротив, има най-висока плътност.
С помощта на теста на Зимницки се определя и дневната диуреза - общото количество урина, отделена през деня. Нормално през деня се отделят около 1,5-2 литра урина. С помощта на теста на Зимницки се определя колко урина е била отделена през деня и колко през нощта. Ежедневните колебания в диурезата (различно количество урина, отделена през деня и през нощта) показват някои аномалии в работата на бъбреците или сърцето.
Как се събира урината за теста на Зимницки?
Събирането на урина за теста на Зимницки се извършва в рамките на един ден. По време на събирането на урина субектът трябва да се храни както обикновено и да приема обичайното количество течност за себе си (за предпочитане не повече от 1,5-2 литра течност на ден). Паралелно със събирането на урина е необходимо да се изчисли количеството приета течност (включително течна храна), тъй като това е важно при изчисляването на резултатите от анализа.
На субекта се дават 8 буркана, във всеки от които след един ден трябва да се събере урина. В 6 сутринта на първия ден субектът изпразва пикочния мехур в тоалетната. След това, точно на всеки 3 часа, трябва да събирате цялата урина в съответния буркан. Така урината се събира в 9, 12, 15, 18, 21, 24, 3 и 6 сутринта на следващия ден. Общо се получават 8 порции урина, по една порция урина във всеки буркан.
Всички буркани с урина, както и данни за това колко течност е изпита през деня, се изпращат в лабораторията. Преди да изпратите проби от урина в лабораторията, препоръчително е да ги съхранявате в хладилник.
Какви са нормите на теста на Зимницки?
С помощта на теста на Зимницки се оценяват няколко параметъра на бъбречната функция: плътност на урината, колебания в плътността на урината през деня, количеството течност, отделена през деня, колебания в количеството течност, отделена през деня и нощта. При нормална бъбречна функция резултатите от теста на Зимницки са както следва:
Количеството отделена урина през деня (дневна диуреза) - 1500 - 2000 ml
Съотношението на количеството течност, отделена от бъбреците, към количеството течност, изпита през деня, е 65 - 80%.
Количеството урина, отделена през деня, значително надвишава количеството на отделената през нощта (2/3 от общата урина през деня, 1/3 през нощта)
Плътността на урината в една или повече порции е не по-малка от 1,020
Значителни колебания в количеството и плътността на урината в различни порции през деня. Например през деня една порция е 300 мл, а през нощта порцията е 50 мл. Или в една порция урина плътността е 1,008, а в другата порция - 1,022.
Интерпретация (декодиране) на резултатите от теста на Зимницки.
При провеждане на тест на Зимницки при хора с увредена бъбречна функция се наблюдават различни отклонения от нормата. Основните нарушения, открити с помощта на теста на Зимницки, са следните:
Ниската плътност на урината е резултат от теста на Зимницки, при който в нито една от порциите плътността на урината не надвишава 1,012-1,013. Ниската плътност на урината се нарича хипостенурия и показва нарушение на концентрационната способност на бъбреците.
Нарушаването на концентрацията на урината възниква при приемане на диуретични лекарства (фуроземид, етакринова киселина и др.), Както и при следните заболявания:
Късните стадии на хронична бъбречна недостатъчност се срещат при хора, които дълго време страдат от определени бъбречни заболявания (гломерулонефрит, пиелонефрит, амилоидоза на бъбреците и др.) При хронична бъбречна недостатъчност се наблюдават следните основни симптоми: влошаване на общото състояние състояние, главоболие, летаргия, загуба на апетит, жажда, лоша миризмаот устата. В биохимичния анализ на кръвта се наблюдава повишаване на нивото на креатинин, урея и др.
Обострянето на двустранен пиелонефрит или възпаление на таза на двата бъбрека също е причина за намаляване на плътността на урината. При пиелонефрит основните симптоми са: периодична болка в лумбалната област, треска до високи цифри, главоболие, гадене и др.
Тежката сърдечна недостатъчност в някои случаи води до увреждане на бъбреците и нарушена концентрация на урина. При лоша сърдечна функция кръвта застоява в бъбреците и други органи, което води до нарушаване на тяхната работа. При сърдечна недостатъчност има тежък задух, слабост, главоболие, подуване на краката, воднянка (асцит).
Безвкусен диабет е заболяване, при което поради липса на специфичен хормон (вазопресин) бъбреците не могат да връщат течността от урината. Тялото губи много течности с урината. Симптомите на безвкусен диабет са: силна жажда, често уриниране, загуба на тегло, суха кожа, голямо количество урина на ден (до 5-10 литра) и др.
Ниската плътност на урината, която практически не се променя в зависимост от времето на деня или количеството приета течност, се нарича хипоизостенурия. При хипоизостенурия плътността на урината във всяка част от теста на Зимницки като правило не надвишава 1,009 и практически не се променя през целия ден. Такъв резултат от теста на Зимницки предполага, че бъбреците не са в състояние да се адаптират към променящите се условия за приемане на течности в тялото и показва тежка бъбречна недостатъчност.
Увеличаването на плътността на урината, като правило, показва проникването в урината на голямо количество плътно вещество (например протеин, глюкоза и др.) Болестите, при които се увеличава плътността на урината, са както следва :
Захарният диабет причинява отделяне на големи количества глюкоза с урината. Наличието на глюкоза в урината увеличава нейната плътност. Като правило, при наличие на глюкоза в урината (глюкозурия), има често уриниране, жажда, загуба на тегло, повишен апетит и други симптоми на диабет.
Остър или хроничен гломерулонефрит е заболяване, при което пропускливостта на гломерулите на бъбреците е нарушена и в урината навлизат големи кръвни вещества: кръвни клетки, протеини. Наличието на протеин в урината се нарича протеинурия. Протеинът е причината за увеличаване на плътността на урината. В допълнение, при гломерулонефрит може да се наблюдава хематурия (наличие на кръв в урината, вижте Анализ на урината според Nechiporenko), болка в лумбалната област, треска и др.
Токсикозата на бременни жени в някои случаи допринася за увеличаване на плътността на урината поради отделянето на протеин в урината.
Както бе споменато по-горе, обикновено човек отделя от 65 до 80% от течността, консумирана през деня. Ако през деня пациентът със сърдечна недостатъчност и оток отдели по-малко от 65% от приетата течност, това показва, че заболяването се влошава и отокът се увеличава. Ако отделянето на урина е повече от 80% от количеството приета течност, състоянието се подобрява, отоците спадат.
Увеличаването на количеството отделена през деня урина над 2000 ml се нарича полиурия и се наблюдава при следните състояния:
Диабетът причинява отделяне на глюкоза в урината, което извлича течност в урината. При диабет се увеличава количеството отделена през деня урина.
Безвкусен диабет е дефицит на хормон, който насърчава задържането на вода в тялото (вазопресин). Липсата на този хормон е причина за големи загуби на вода с урината.
Бъбречна недостатъчност възниква при хора с бъбречно заболяване. При бъбречна недостатъчност бъбреците не са в състояние да концентрират урината, което води до повишено отделяне на течност в урината.
Тестът на Reizelman е модификация на теста на Zimnitsky, според който събирането на урина се извършва на свободни интервали от време. Използван в детството.
При запазената способност на бъбреците за осмотично разреждане и концентрация на урина се отбелязват следните:
Значителни колебания в обема на урината в отделни порции (50-250 ml);
Максималната относителна плътност, характеризираща способността на бъбреците да концентрират урината, не трябва да бъде по-ниска от 1025 g/l;
Минималната относителна плътност, която отразява способността на бъбреците за осмотично разреждане на урината, при здрав човек трябва да бъде по-ниска от осмотичната концентрация (осмоларност) на безпротеинова плазма, равна на 1010-1012 и обикновено е 1003-1006;
Значителни колебания в относителната плътност на урината: разликата между максималните и минималните стойности трябва да бъде най-малко 12-16 единици. (например от 1006 до 1020 или от 1010 до 1026 и т.н.); значителните дневни колебания в относителната плътност на урината са свързани със запазената способност на бъбреците да концентрират или разреждат урината в зависимост от постоянно променящите се нужди на тялото;
Явно (приблизително двукратно) преобладаване на дневната диуреза над нощната.
3. Тестове за натоварване. Тест за концентрация.
Обектът е на суха диета за 12-24 часа. Водата, плодовете, плодовете, зеленчуците са изключени от диетата, включени са ронливи зърнени храни, бисквити, твърдо сварено яйце, извара и месо. Проучването започва в 15.00 часа, пикочният мехур се изпразва, след което се събира урина на всеки 3 часа, определя се количеството на урината, относителната плътност или осмотичността. Крайното време на пробата се определя при получаване на резултатите (достигане на ниво на специфично тегло от 1025 g/l и повече), както и като се вземе предвид благосъстоянието на пациента.
* деца ранна възраст
* заболявания на централната нервна система
* активност на възпалителния процес в бъбреците
* бъбречна недостатъчност
* метаболитна нефропатия (включително невро-артритна диатеза).
В основата на нарушението на концентрационната способност на бъбреците е намаляването на осмотичното налягане в тъканта на медулата на бъбреците. Това може да се дължи както на увреждане на самите бъбреци, така и на екстраренални фактори (Таблица 2).
С прогресирането на бъбречното заболяване намаляването на способността за концентрация се комбинира с нарушение на способността на бъбреците да се разреждат.
4. Тестове за натоварване. Тест за водно натоварване.
По време на изследването не се дава храна, пациентът е на полупостелен режим. използване сварена водастайна температура 20 мл/кг, която се изпива за 15-30 минути. След това пикочният мехур се изпразва и урината се събира на всеки 30 минути в продължение на два часа (4 порции) и още 1-2 часа след час (1-2 порции). За да се получи продължителна максимална диуреза, в началото на всяко редовно събиране на урина, на детето се дава да изпие количество вода, равно на обема на урината, получена за предходния период, плюс количеството вода за екстраренални загуби.
Противопоказания за теста:
* едематозен синдром
* хипертоничен синдром
* сърдечна недостатъчност
* състояния, придружени с тахикардия.
Тълкуване на резултатите:
През първите два часа здраво дете отделя най-малко 70% от изпитата течност, докато относителната плътност на урината намалява (до 1001-1005 g / l);
С намаляване на способността на бъбреците да разреждат урината, стойностите на относителната плътност не достигат тези показатели (обикновено 1004-1009 g / l);
При пълна загуба на функцията на разреждане, относителната плътност е на ниво 1010-1012 g / l, т.е. съответства на осмотичната концентрация на плазмата (изостенурия).
Олигурията, дължаща се на нарушена бъбречна функция, в повечето случаи се комбинира с намаляване на осмоларитета (или специфичното тегло) на урината. Олигурията при пациенти със запазена бъбречна функция е придружена от урина с нормално или повишено специфично тегло.
Стрес тестовете позволяват да се оцени функционалното състояние на бъбреците и техните резервни възможности, но наличието на редица противопоказания (включително ранна детска възраст) ограничава тяхното използване.
Понастоящем дезмопресин (синтетичен аналог на естествения антидиуретичен хормон аргинин-вазопресин) се използва за оценка на концентрационната функция на бъбреците. В сравнение с естествения хормон дезмопресинът има по-мощно и продължително действие и няма изразен вазоконстрикторен ефект.
Една от дозираните форми на дезмопресин е Precynex, дозиран спрей за нос. Според резултатите от чуждестранни многоцентрови проучвания, лекарството се отличава с висока точност на дозиране, удобна форма на освобождаване, безопасна и ефективен начинприложение, не предизвиква атрофия на носната лигавица.
Дозите на Precynex за теста за бъбречна концентрация зависят от възрастта:
Средна доза
Възрастни - 40 mcg / ден
Деца до една година - 10 mcg / ден
Деца над една година - 10-20 mcg / ден
Провеждането на тест за концентрационната способност на бъбреците с помощта на Precynex осигурява последователно изпълнение на следните условия:
* Изпразва се пикочния мехур (излива се първата порция). Повторното вземане на проби от урина се извършва 4 часа след първото изпразване на пикочния мехур.
* Повторно вземане на урина - след 4 часа.
*За определяне на осмоларитета се събират само две порции урина в рамките на 8 часа.
* По време на изследването ограничете количеството приета течност (обемът на течността, получен 1 час преди изследването и в рамките на 8 часа след него, не трябва да надвишава 0,5 литра).
Получените резултати се оценяват по отношение на осмоларитета.
* Нормата на осмоларитет за възрастни е до 1200 mOsm / kg H2O.
* При деца скоростта на осмоларитет е 600 mOsm / kg H2O (трябва да се достигне в рамките на 5 часа след приложението на лекарството).
* Ако установеният осмоларитет е под посочените стойности, тогава тестът трябва да се повтори. Повторното идентифициране на нисък показател показва нарушение на концентрационната способност на бъбреците. В този случай пациентът се нуждае от допълнителен задълбочен преглед.
По този начин използването на Precynex е нов неинвазивен метод за диагностициране на нарушения на концентрационната функция на бъбреците, включително при малки деца.
Литература
1. Материали на руската научно-практическа конференция "Актуални проблеми на детската нефрология". - Оренбург, 21 - 23 май 2010 г. - Оренбург, 2010 г.
2. Наточин Ю. В. Въведение в нефрологията / Ю. В. Наточин, Н. А. Мухин. - ООО Аргумент, ГЕОТАР-МЕДИА, ИЗДАТЕЛСКА ГРУПА, 2007 г. - 160 с.
3. Нефрологията в терапевтичната практика / Ed. А. С. Чижа. - Минск: Висше училище, 1998. - 557 с.
4. Papayan A. V. Ръководство по клинична нефрология за лекари / A. V. Papayan, N. D. Savenkova. - Санкт Петербург: СОТИС, 1997. - 720 с.
5. Справочник по соматични заболявания
Хоствано на Allbest.ru
Подобни документи
Морфо-функционални характеристики на отделителната система. Анатомия на бъбреците. Структурата на бъбреците. Механизъм на уриниране. Кръвоснабдяване на бъбреците. Нарушение на функциите на отделителната система при патология, пиелонефрит. Методи за изследване на урината и бъбречната функция.
резюме, добавено на 31.10.2008 г
Етиология и патогенеза на нарушена бъбречна функция: гломерулна и тубулна филтрация, реабсорбция, секреция, концентрация и разреждане на урината. Клинична диагностика на бъбречни заболявания, лабораторни изследвания и анализ на физикални и химични свойстваурина.
курсова работа, добавена на 15.06.2015 г
Характеристики на бъбречната патология. Чести причини за бъбречна дисфункция. Проява на нарушения на уринирането и уринирането. Прояви на бъбречни нарушения. Механизми на нарушена бъбречна екскреторна функция. Основните видове бъбречна патология по произход.
презентация, добавена на 05.03.2017 г
Механизми на образуване на урина. Бъбречни и екстраренални пътища на екскреция на веществата. Основни функции на бъбреците. Кръвоток в различни части на бъбреците. Структурата на кръвоносната система. Класификация на нефроните. Механизми на уриниране. Филтрация, реабсорбция, секреция.
презентация, добавена на 01/12/2014
Проучване на оплакванията на нефрологични пациенти, събиране на анамнеза при пациент със съмнение за бъбречно заболяване. Преглед на причините за обостряне, естеството на хода на заболяването, палпация. Анализ количествени методиизследване на седимента на урината, синдром на бъбречна недостатъчност.
презентация, добавена на 25.12.2011 г
Структурата на органите на пикочната система на човека: пикочен мехур, уретери, таз, бъбречни чашки, уретра. Етапи на метаболизма в организма. Отчитане на функциите на бъбреците: отделителна, защитна и поддържаща хомеостазата.
презентация, добавена на 15.04.2013 г
Разглеждане на синдрома на нарушена бъбречна функция, водещ до нарушение на водния, електролитния, азотния и други видове метаболизъм. Критерии на RIFLE за диагностика и класификация на остро бъбречно увреждане. Стандартизиране на определенията за увредена бъбречна функция.
презентация, добавена на 30.05.2014 г
Интероцептивна функция на бъбреците. Изследване на влиянието на един бъбрек върху друг. Ролята на бъбречната рецепция в развитието на хипертония. Денервиран бъбрек. Ролята на вагусните нерви в осъществяването на рефлексни реакции, насочени към поддържане на йонния баланс.
резюме, добавено на 06/01/2010
Топография на бъбреците, тяхната скелетотопия. Характеристики на топографската анатомия на бъбреците, бъбречните съдове, уретерите и пикочния мехур в детска възраст. Солитарни кисти на бъбреците. Последици и причини за развитие на хипоплазия. Патология на удвояването на бъбреците, нейните видове.
презентация, добавена на 07.09.2015 г
Основни функции на бъбреците. Правила за събиране на урина за изследване. Цвят, мирис, киселинност на урината, съдържание на глюкоза, еритроцити, левкоцити и протеин в нея. Функционална и патологична протеинурия. Прояви на нефротичен и азотемичен синдром.
Нарушенията на концентрационната способност на бъбреците при различни състояния (жажда, водно натоварване) и с промени в плазмения осмоларитет се проявяват с хипостенурия, изостенурия и астенурия.
Хипостенурия -ограничаване на концентрационната способност на бъбреците с различен осмоларитет на урината (от максимум до минимум). В този случай специфичното тегло на урината може да достигне 1,025, а осмоларитетът на урината - 850 mmol / l. изостенурия- състояние, характеризиращо се с изразено ограничаване на концентрационната функция на бъбреците, докато специфичното тегло на урината не надвишава 1,010, а осмоларитетът на урината е 300 mmol / l. Астенуриясе нарича състояние, при което концентрационната способност на бъбреците всъщност е напълно нарушена. Специфичното тегло на урината не надвишава 1,001, осмоларитетът на урината е под 50 mmol/L.
В основата на нарушенията на концентрационната способност на бъбреците могат да бъдат метаболитни, ендокринни, хемодинамични, морфологични промени в бъбреците. Намаляването на осмотичния градиент между тубулната урина и медулата е от съществено значение. Така че, при осмотична диуреза в тубулната урина ще се задържи излишно количество осмотично активни, нерезорбируеми вещества (например манитол, урея, глюкоза - над бъбречния праг), които предотвратяват изтичането на течност от лумена на тубула в интерстициума.
Концентрационната способност на бъбреците е намалена при недохранени пациенти, тъй като поради липсата им на енергия и транспортни АТФази, движението на вещества срещу концентрационния градиент от тубулната урина, която има нисък осмоларитет, в медулата се забавя.
Реабсорбцията на натрий в дисталните тубули е нарушена по време на хипоксия, хипотермия и диуретици, което предотвратява развитието на хиперосмоларност в бъбречния паренхим. Напротив, алдостеронът допринася за развитието на хиперосмоларност в бъбречната тъкан.
Нарушенията на бъбречната хемодинамика с повишаване на системното артериално налягане, ограничаване на бъбречния кръвен поток, възпалителна хиперемия при тубулоинтерстициален нефрит могат да причинят намаляване на осмотичния градиент и по този начин да допринесат за намаляване на концентрационната функция на бъбреците.
Увреждането на тубулните клетки е придружено от промени в състава и обема на урината. Дисфункцията на проксималните тубули се проявява чрез намаляване на секрецията на [Н +] йони и реабсорбцията на бикарбонати и вода, последното поради блокадата на противотоковия механизъм и отделянето на голям обем разредена урина. В този случай, като правило, способността на клетките на дисталните тубули и събирателните канали да реагират на ADH се губи. Тежки нарушения на концентрационната функция на бъбреците се наблюдават при дефицит на ADH или липса на чувствителност към този хормон на тубулните клетки. Това заболяване се нарича безвкусен диабет,който е от централен и бъбречен произход. За целите на диференциалната диагноза на тези две състояния се провежда тест за натоварване със сол, за да се установи оставащата чувствителност на бъбречните тубулни клетки към ADH и способността за концентриране на урината.
Когато нефроцитите са увредени, чувствителността на клетките към алдостерон намалява и метаболитните механизми, включващи натрий, се блокират. В урината концентрацията на натрий се увеличава непропорционално в сравнение с кръвната плазма.
Увреждането на проксималните тубули е придружено от намаляване на калиевата реабсорбция и съответно хипокалиемия. Нарушаването на реабсорбцията на глюкоза, фосфати, аминокиселини, урати води до намаляване на нивото им в кръвта и тъканите и съответно до промяна в метаболизма.
По този начин, ако тубулите са повредени във венозната кръв, изтичаща от бъбреците, се определят киселинно рН, хипокарбонатемия, хипокалиемия, хипофосфатемия, хипоурикемия и нормални нива на урея и креатинин. Обемът на урината се увеличава, съдържа относително висока концентрация на натрий, дори при намален бъбречен кръвоток, и непропорционално ниска концентрация на урея.